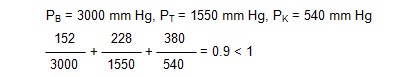1. Bütan (B) ve pentan (P) karışımı dengededir; basınç 3
atm ve sıcaklık 100 0F dır. Sıvı ve gaz karışımlarının
bileşimlerini,
a. Rault Kanunu yoluyla,
b. Deneysel K değerleri ve Y
= KX formülünden
yararlanarak hesaplayınız.
Buhar-basınç tablolarından, 100 0F da,
PB = 2650 mm Hg, PP
= 830 mm Hg
P = 3 atm basınç ve T = 100 0F için K
değerleri grafiklerden,
KB = 1.15 KP
= 0.36
Çözüm:
a.
Bu sonuçlar birbirine çok yakındır. Bu durum, 3 atm
basınçta, bütan + pentan karışımı için Rault Kanununun uygulanabilirliğini
gösterir.
2. 100 0F
sıcaklık ve 465 psia basınçta bütanın (B) pentana (P) göre relatif uçuculuğu (aBP) nedir?
a. Rault Kanunu yoluyla,
b. Deneysel K değerlerinden yararlanarak hesaplayınız.
Buhar-basınç tablolarından, 100 0F da,
PB = 2650 mm Hg, PP
= 830 mm Hg
P = 465 psia basınç ve T = 100 0F için K
değerleri grafiklerden,
KB = 0.24, KP
= 0.085
Çözüm:
a. İkili bir sistemde, Rault kanunu
geçerli olduğunda,
3. Mol olarak %20 benzen, %30 toluen ve %50 o-ksilen
içeren gaz karışımındaki gazların çiğlenme noktalarını bulunuz; basınç 1
atmosferdir.
Çözüm:
P = 1 atm de Rault kanunu uygulanabilir. Karışımdaki üç
bileşenin buhar basınçları sıcaklığa bağlıdır. Burada deneme-yanılma yöntemi
uygulanır.
Benzen için,
o-Ksilen için,
2. T = 270 0F
3. T = 263 0F
4. Mol olarak %40 etilen, %60 propilen içeren gaz
karışımındaki gazların çiğlenme noktasını, deneysel K değerleri ve Y = KX
formülünden yararlanarak hesaplayınız; basınç 31.6 atmosferdir.
P= 31.6 atm, Etilen, YE
= 0.40, Propilen, YP = 0.60
Çözüm:
Burada deneme - yanılma (veya, yaklaştırma) yöntemi
uygulanır.
Ek-23’teki eğrilerden, seçilen bazı sıcaklıklardaki K
değerleri okunur. Her bir K değeri için YE = 0.40, YP =
0.60 olduğunda XE ve XP değerleri hesaplanır.
Çiğlenme nokrasında,
XE + XP @ 1
olması gerektiğinden, bu değere en yakın sonuçların elde
edildiği sıcaklık çiğlenme noktası olarak alınır.
Seçilen sıcaklıklar, aşağıdaki tablolarda da görüldüğü gibi,
100, 20, 160, 140, 120 ve 110 0F.
5.
Aşağıda isimleri verilen maddelerden oluşan üçlü karışım sıvı halde bulunmaktadır.
Karışımı oluşturan maddelerin karışımdaki mol kesirleri, karşılarında
verilmiştir. P = 15 psia basınçta bu karışımın kaynama noktasında
(kabarcıklanma noktası) oluşan ilk buhar fazının bileşimini (mol kesirlerini)
bulunuz.
n-Heksan
(n-C6) mol kesri: 0.25, n-Heptan (n-C7) mol kesri: 0.40, n-Oktan
(n-C8) mol kesri: 0.35, p = 15 psia
Çözüm:
Y = K X ve Y1 + Y2 + Y3
= 1.0
olduğu zaman kabarcıklanma noktasına gelinmiş olacaktır.
6. Sürekli basit distilasyonla, aşağıda bileşimi verilen üçlü karışım, 5000 mol/sa lik bir akım hızıyla kolona beslenerek saflaştırılmaktadır. Kolon basıncı p = 40 psia olup destilasyon sonucunda beslemenin % 45 i kolon tepesinden gaz akımı olarak alınmaktadır. Bu işlemde oluşan gaz ve sıvı akımlarının bileşimlerini (mol kesirlerini) ayrı ayrı bulunuz.
Propan
(C3) mol kesri: 0.25, n-Bütan (n-C4) mol kesri: 0.40, n-Pentan
(n-C5) mol kesri: 0.35, p = 40 psia, V = % 45 = 2250 mol/sa, L =
2750 mol/sa, F = 5000 mol/sa
Çözüm:
7.
Aşağıda isimleri verilen maddelerden oluşan üçlü karışım gaz halde bulunmaktadır.
Karışımı oluşturan maddelerin karışımdaki mol kesirleri, karşılarında
verilmiştir. p = 100 psia basınçta bu karışımın çiğlenme noktasında oluşan sıvı
fazının bileşimini (mol kesirlerini) bulunuz.
Çözüm:
Etilen (C2-)
mol kesri: 0.25, Etan (C2) mol kesri: 0.40, Propilen (C3-)
mol kesri: 0.35, p = 100 psia
8.
Aşağıdaki maddelerden oluşan üçlü bir karışım sürekli basit destilasyon
işlemine tabi tutulmaktadır. Karışım kolona toplam 2500 mol/sa lik bir akım ile
beslenmektedir. Beslenme içindeki her bir maddenin mol kesirleri aşağıda
verilmektedir. Kolon basıncı p = 80 psia olup destilasyon sonucunda beslemenin
%55 miktarı kolon dibinden sıvı akımı olarak alınmaktadır. Bu işlemde oluşan
gaz ve sıvı akımlarının bileşimleri (mol kesirleri) bulunuz.
Propilen
(C3-) mol kesri: 0.45, L
= % 55 V = % 45, F = 2500 mol/sa
Propan
(C3) mol kesri: 0.40, L = 1375 mol/sa, V = 1125 mol/sa
n-Bütan
(n-C4) mol kesri: 0.15, L = f / (1 + KV / L), p = 80 psia
Çözüm:
9. Bir
destilasyon kolonuna aşağıdaki tabloda verilen kompozisyonda F = 2500 mol/sa
besleme girmektedir.
Kolon
basıncı 80 psia, besleme akımının sıcaklığı T = 45 0C olup kolona
giriş noktasında besleme akımı %45 oranında buharlaşmış bulunmaktadır. Kolonun
tepesindeki toplam konderserden alınan ürün miktarı ve bileşimi aşağıda
verilmektedir.
Besleme akımı, XF
|
Tepe ürün akımı,
XD = 1425 mol/sa |
|
Propilen:
|
0.45
|
0.77
|
Propan:
|
0.40
|
0.21
|
n-Butan:
|
0.15
|
0.02
|
Kolonda bulunan reflüks oranı L/D= 2 dir. Bu şartlar altında yapılan bir fraksiyonlu destilasyon işleminin sürdürüldüğü tepsili kolon ile ilgili olarak;
a.
Kolonun besleme noktası altındaki ve üstündeki bölümlerde (Stripper ve
rectifier bölümleri) olması gereken sıvı ve gaz akımlarının (V, L, V, L) miktarlarını
bulunuz. (10 puan)
b. Tepe
ve dip ürünlerinin ayrı ayrı bileşimlerini miktar ve mol kesri olarak
hesaplayınız.
Çözüm:
a. F = 2500 mol/sa
10. Mol olarak %15 propilen, %40 propan, % 25 n-bütan ve
%20 n-pentan içeren çoklu gaz karışımındaki gazların çiğlenme noktasını,
deneysel K değerleri ve Y = KX formülünden yararlanarak hesaplayınız; basınç
465 psi (31.6 atm) dir.
Çözüm: p = 465 psi (31.6 atm)
Burada deneme –yanılma (veya, yaklaştırma) yöntemi
uygulanır. Ek-23’teki eğrilerden, seçilen bazı sıcaklıklardaki K değerleri
okunur. Her bir K değeri için, YP- = 0.15, YP
= 0.40, YB- = 0.25 ve YP = 0.20 olduğunda XP-,
XP, XB ve XP değerleri hesaplanır. Çiğlenme
nokrasında,
olması gerektiğinden, bu değere en yakın sonuçların elde
edildiği sıcaklık çiğlenme noktası olarak alınır. Seçilen sıcaklıklar,
aşağıdaki tablolarda da görüldüğü gibi, 200, 300, 380, 260, ve 265 0F
dır.
Çiğlenme noktasının, T = 260 0F ile 265 0F arasındaki değişimin doğrusal olduğu kabul edilerek T = 262 0F = 127.8 0C olduğu bulunur.
Çiğlenme noktasının, T = 260 0F ile 265 0F arasındaki değişimin doğrusal olduğu kabul edilerek T = 262 0F = 127.8 0C olduğu bulunur.
11.
Aşağıdaki maddelerden oluşan dörtlü bir karışım sürekli basit destilasyon
işlemine tabi tutulmaktadır. Karışım kolona toplam 800 mol/sa lik bir akım ile
beslenmektedir. Besleme içindeki her bir maddenin mol kesirleri aşağıda verilmektedir.
Kolon basıncı p = 50 psia olup destilasyon sonucunda beslemenin % 35 miktarı
kolon tepesinden gaz akımı olarak alınmaktadır. Bu işlemde oluşan gaz ve sıvı
akımlarının bileşimlerini (mol kesirlerini) ayrı ayrı bulunuz.
F = 800
mol/sa, p = 50 psia, V = % 35 = 280 mol, L = % 65 = 520 mol
12. Bir
denge kademesinde gaz fazını aşağıdaki maddeler karşılarında gösteren
miktarlarda oluşturmaktadır. P = 350 psi basınç altında bulunan sistemin
kabarcıklanma sıcaklığını bulunuz.
Metan:
160 mol/sa, etilen: 1040 mol/sa, etan: 320 mol/sa, propilen: 80 mol/sa, p = 350
psi
Çözüm:
13.
Sürekli basit destilasyonda (flush destilasyon) besleme akımı aşağıdaki
maddelerden oluşmaktadır.
Etilen: % 60, Etan: % 5, Propan: % 30, n-Bütan: % 5
Distilasyon
işleminden elde edilen tepe akımı (V) beslemenin (şarjın) % 70 ini ve dip akım
(L) ise % 30 unu oluşturmaktadır. p = 150 psi de yapılan bu destilasyon
sonundaki buhar ve sıvı fazlarının(tepe ve dip akımlarının), (a) Oluşturduğu
denge kademesinin sıcaklığını, (b) Akımların bileşimlerini X ve Y değerleri
olarak bulunuz.
Çözüm:
p = 150 psi, V = 70, L = 30
14. Üstü açık, silindirik bir tank, üst seviyenin 2 inç
altına kadar saf metanolle doldurulmuştur. Tank, şekilde görüldüğü gibi, yukarı
kısımda daralmaktadır. Tank içinde kalan hava durağandır, fakat tankın
üstündeki hava sirkülasyonu nedeniyle bir miktar metanol kaybı olmaktadır. Tank
ve hava 77 0F sıcaklık ve 1 atm basınçtadır; bu koşullarda metanolün
difüzivitesi 0.62 ft/sa. Kararlı halde, tanktaki metanol kaybını hesaplayınız.
Çözüm:
Metanol, sıvı seviyesinden itibaren 2 ft yüksekliğe kadar
olan durağan hava içine difüzlenir. Transfer alanı değişkendir. Sıvı
seviyesindeki havada bulunan metanol konsantrasyonunu, metanolün 77 0F
sıcaklıktaki buhar basıncı belirler; bu dğer pa = 135 mm Hg dir.
(Na = kütle transfer hızı, lb mol/sa, c= mol) Bu
eşitliğin integralinde A nın x cinsinden ifade edilmesi gerekir.
15. Mutfak eviyesi suyla doldurulup içine yağlı bir kap
konulduğunda, kaptaki yağ ince bir film tabakası halinde suyun üstüne çıkar.
Eviyenin derinliği 18 cm, tabak üzerindeki yağın konsantrasyonu 0.1 mol/cm3
dür ve başlangıçta eviyenin üst kısmında
yağ olmadığı kabul ediliyor. Yağ damlacıklarının sudan geçerek yüzeye doğru
akısı, J nedir?
Difüzyon katsayısı, D = 7 x
10-7cm2/s dir.
Çözüm:
Fick Kanunu:
16. Titanyum, karbon difüzlenerek sertleştirilmektedir.
Titanyum levhanın yüzeyinden 1 mm derinlikteki karbon konsantrasyonu 0.25 kg/m3,
3 mm derinlikteki ise 0.68 kg/m3 dür. Karbonlaştırma ortamının
sıcaklığı 925 0C ve karbonun 2 mm kalınlıktaki bölgeye girme hızı J
= 1.27 x 10-9 kg/(m2 s) dir. Bu işlemdeki difüzyon
katsayısı (D) nedir?
Çözüm:
Fick I. Kanunu,
17. Paslanmaz çelik ve nikel alaşımı, ortam sıcaklığı
1500 0C de 12 saat bekletiliyor. Başlangıçta alaşımdaki nikel
konsantrasyonu ağırlıkça % 0.30 ve yüzeydeki konsantrasyonu % 0.80 dir. Çelik
içinde 0.5 mm derinlikteki nikel miktarının ağırlıkça % 0.50 olması için ne
kadar zaman gerekir? Nikelin çelikteki difüzivitesi, 1500 0C de, D
= 4.34 x 10-13 m2/s
dir. Hata faktörü (erf): z1
= 0.55 için, erf(z)1 = 0.5633; z2 = 0.60 için, erf(z)2
= 0.6039 dur.
Çözüm:
Burada kararsız hal difüzyon söz konusu olduğundan yüzey
konsantrasyonu sabittir.
18. Bir demir-karbon alaşımı ağırlıkça %0.25 karbon
içermektedir. Bu alaşım 950 0C (1750 0F) sıcaklıkta
tutulduğunda yüzeydeki karbon konsantrasyonu hemen %1.20 (ağ.) değerine
yükseliyorsa, yüzeyden 0.5 mm derinlikteki karbon konsantrasyonunun %0.80 (ağ.)
olabilmesi için ne kadar zamana gereksinim vardır?
Karbonun, bu sıcaklıkta, demir içindeki difüzyon
katsayısı 1.6 x 10-11 m2/s.dir. Hata faktörü (erf): z1 =
0.35 için, erf(z)1 = 0.3794; z2 = 0.40 için, erf(z)2
= 0.4284 dür.
Çözüm:
Burada kararsız hal difüzyon söz konusu olduğundan yüzey
konsantrasyonu sabittir.
19. 27.0 0C sıcaklığındaki su damlalarının,
damlaları saran 48.4 0C deki havayla buharlaştırılması isteniyor;
havanın akış hızı v = 1.0 m/s, çevre havasının ıslak hazne sıcaklığı 21.5 0C,
kuru hazne sıcaklığı 26.0 0C dir. Su damlalarının ilk çapı, D =
0.002052 m ve kütlesi = 4.522 x 10-3 g dır. Deneysel olarak saptanan
kuruma zamanı t = 354 s ve buharlaşma ısısı, Nc = 1.28 x 105
g/s dir.
a. Buharlaşma hızını enerji dengesi metoduyla
hesaplayınız.
b. Buharlaşma hızını kütle transferi/difüzyon metoduyla
hesaplayınız.
c. Çalışma parametrelerinin etkisini, aşağıda verilen
değerlerde olması halinde, inceleyiniz
Çözüm:
a. Enerji Dengesi Metodu
Konvektiv ısı transfer katsayısı aşağıdaki eşitlikten
hesaplanır.
Su damlasının buharlaşma ısısı,
b. Kütle Transferi / Difüzyon Metodu
Küre şeklindeki bir damladan, sıcak hava akımıyla kütle transferinde
Sherwood sayısı (NSH) ilişkisinden yararlanılır.
Su damlalarının ilk
çapı, D = 0.002052
µa =
19.46 x 10-6 kg/ms, ρa = 1.098 kg/m3, v
= 1.0 m/s
Kütle transfer katsayısı, kc
c. Çalışma Parametrelerinin Etkisi
1. Hava neminin
etkisi:
Mutlak nemin 0.016
kg H2O/kg kuru hava değerine yükseltilmesi halinde,
2. Çalışma basıncının etkisi:
Çalışma basıncı, normal atmosfer basıncının yarısı kadar, pçalışma
= 50662 Pa olması halinde,
3. Hava akım hızının etkisi:
Hava akım hızının 5.0 m/s değerine çıkarıldığını varsayalım.
4. Hava sıcaklığının etkisi:
Hava sıcaklığı 71.85 0C olduğunda, aşağıdaki
parametreler geçerlidir:
Yorum:
1. Hava neminin artmasıyla buharlaşma hızı düşer.
2. Çalışma hava basıncının düşmesiyle buharlaşma hızı artar.
3. Hava ve damla arasındaki hava akış hızının (relatif hız)
artmasıyla buharlaşma hızı artar.
4. Hava sıcaklığının yükselmesiyle buharlaşma hızı artar.
5. Damlaların kuruma performansında, yukarıdaki dört etkin
faktör arasında, hava sıcaklığı (4) ve hava akış hızı (3) en önemli
etkenlerdir.
20. a. %80 su içeren bir gıda madde atmosfer basıncında, 100 0C
de havayla kurutularak su miktarının %10 a düşürülmesi isteniyor. Gıda
maddesinin ilk sıcaklığı 210C olduğuna göre, orijinal halinin birim
ağırlığı için gereken ısı enerjisi ve kadardır? Uzaklaştırılan 1 kg su için
harcanan enerji (Q) ne kadardır?
b. Madde, vakumda 20 kPa mutlak. (veya 81.4 kPa vakum)
basınc ve 60 0C de kurutulduğunda, birim ağırlık başına
uzaklaştırılan nem miktarı için gereken ısı enerjisi (Q) ne kadar olur?
c. Maddenin 0 0C de dondurulmuş ise, 0 0C
den başlayarak hammaddenin birim ağırlığı başına gereken enerji miktarı (Q)
nedir?
Maddenin spesifik ısı kapasitesi: cp = 3.8 kJ/(kg 0C)
Suyun spesifik ısı kapasitesi: cpsu = 4.186 kJ/(kg 0C) dir.
Suyun 100 0C ve 1 atm. basınçtaki buharlaşma ısısı: lb1 = 2257 kJ/kg
Suyun 60 0C ve 20 kPa basınçtaki buharlaşma ısısı: lb2 = 2358 kJ/kg
Buzun 0 0C ve 1 atm. basınçtaki süblimasyon ısısı: ls = 2838 kJ/kg
Maddenin spesifik ısı kapasitesi: cp = 3.8 kJ/(kg 0C)
Suyun spesifik ısı kapasitesi: cpsu = 4.186 kJ/(kg 0C) dir.
Suyun 100 0C ve 1 atm. basınçtaki buharlaşma ısısı: lb1 = 2257 kJ/kg
Suyun 60 0C ve 20 kPa basınçtaki buharlaşma ısısı: lb2 = 2358 kJ/kg
Buzun 0 0C ve 1 atm. basınçtaki süblimasyon ısısı: ls = 2838 kJ/kg
Çözüm:
a. Kurutulacak
gıda maddesinin 1 kg miktarı için:
Nem miktarı = %80: 800 g su, 200
g kuru madde
Kurutulmuş maddenin 1 kg miktarı için,
Nem miktarı = %10: 100 g su, 900
g kuru madde
100 x 200 / 900 = 22.2 g nem; 200
g kuru madde
1 kg orijinal madde için,
800 – 22.2 = 777.8 g nem ~ 778 g = 0.778 kg nem
Kurutulacak maddenin 1 kg miktarı için gerekli ısı enerjisi,
Q,
Q = sıcaklığı 100 0C ye yükseltmek için ısı
enerjisi + suyun buharlaşma ısısı
Q = mürün (T2 – T1) cp + msu lb1
Q = 1 x (100 - 21) x 3.8 + 0.778
x 2257
Q = 300.2 + 1755.9 = 2056 kJ
enerji / uzaklaştırılan kg su = 2056
kJ / 0.778 kg = 2643 kJ/kg
b. Kurutulacak
maddenin 1 kg miktarı için gerekli ısı enerjisi, Q,
Q = sıcaklığı 60 0C ye yükseltecek ısı enerjisi + suyun 20 kPa da buharlaşma ısısı
Q = mürün (T2 – T1) cp + msu lb2
Q = 1 x (60 - 21) x 3.8 + 0.778 x 2358
Q = 148.2 + 1834.5 = 1983 kJ
c. Donmuş bir
maddenin kurutulmasında süblimasyon ısısı dikkate alınmalıdır; süblimasyon ısısında
basınç etkisi çok azdır.
Kurutulacak maddenin 1 kg miktarı için gerekli ısı enerjisi,
Q,
Q = m x ls
Q = 0.778 kg x 2838 kJ/kg = 2208
kJ
21. 100 kg ürünün nem miktarı bir kurutucuda %80 den %10
a düşürülmektedir. İşlemde, 49800 m3 havanın 80 0C ye
ısıtılması için 70 kPa basınçlı 250 kg buhar kullanılmaktadır. Kurutucudan
geçen havanın sıcaklığı 71 0C ye düşmektedir. Ürün kurutucuya, çevre
sıcaklığı olan 24 0C de girmekte ve kurutucuyu, kurutucudan çıkan
havanın sıcaklığı olan 71 0C de terk etmektedir. Kurutucunun verimi
nedir?
Suyun 71 0C deki
buharlaşma ısısı: lsu = 2331 kJ/kg
Buharın 70 kPa da yoğunlaşma
ısısı: lbuhar = 2283 kJ/kg
Ürünün spesifik ısısı: cpürün
= 3.43 kJ/(kg 0C),
Havanın spesifik ısısı: cphava
= 1.0 J/(kg 0C)
Havanın yoğunluğu: rhava = 1.06 kg/m3
Çözüm:
100 kg hammaddede %80 nem olduğuna göre,
su =100 x 0.80 = 80 kg
kuru madde = 100 x 0 20 = 20 kg
Nem miktarının %10 olması isteniyor,
toplam kuru madde = 20 x (10/9) =
22.2 kg
su = (22.2 – 20) = 2.2 kg
uzaklaştırılan su = (80 – 2.2) =
77.8 kg.
100 kg ürüne verilecek ısı, ürünün sıcaklığını 24 0C den 71 0C ye yükseltmek için gerekli olan ısı ile suyun buharlaşma ısısının toplamına eşittir.
100 kg ürüne verilecek ısı,
Qürün = mürün
(T2 – T1) cp
+ msu lsu
Qürün = 100 x (71 - 24) x 3.43 + 77.8 x 2331
Qürün = 16 x 103 + 181 x 103 =
1.97 x 105 kJ.
Sadece suyu buharlaştırmak için verilecek ısı,
Qsu = 77.8 x 2331 =
1.81 x 105 kJ
100 kg ürünün kurutulması için havanın verdiği ısı,
cphava = 1.0 J/(kg 0C)
rhava
= 1.06 kg/m3,
Qhava = mürün
cp (T2 – T1) mhava
Qhava = 1.0 J/(kg 0C) x (80 - 71) 0C x 49800 m3
x 1.06 kg/m3
Qhava = 100 x1.0 x 10-2
(80 - 71) x 49,800 x 1.06 = 4.75 x 105 kJ.
250 kg buharın enerjisi, buharın 70 kPa daki yoğunlaşma ısısı lbuhar = 2283 kJ/kg olduğuna göre,
Qbuhar = m x lbuhar
Qbuhar = 250 x 2283 =
5.71 x 105 kJ.
Bu sonuçlara göre,
a. Sadece buharlaşma ısısına dayanan verim,
22. Bir
gaz karışımındaki hidrojen suda çüzülmek isteniyor: Toplam basınç 101.3 kPa
(760 torr, 1 atm) olduğunda, 100 g suda çözünebilen hidrojen ne kadardır?
Hidrojenin kısmi basıncı 26.7 kPa (200 torr), sıcaklığı 20 0C dir. H
nin kısmi basıncı, 20 0C de 6.92 x 106 kPa (6.83 x 104
atm)
Çözüm:
Henry
Kanununa göre,
23. Bir klor-hava
karışımında mol fraksiyonu olarak klor 0.503 hava 0.0403 dür. Karışımdaki klor
konsantrasyonunun 0.537 kg/(s m2), veya 396 lb mol /(sa.ft2)değerine
düşürülebilmesi için kolon dolgu maddesi yüksekliği ne kadar olmalıdır? kG
a yBM = 0.1175 k mol/(s m3), veya 26.4 lb mol/(sa.ft2)
tür. Denge geri basıncı yi ihmal ediliyor.
Çözüm:
Kütle transfer katsayısının, lokal gaz kütle hızının 0.8 nci
kuvvetiyle değiştiği varsayılıyor, bu durumda,
Havanın
akış hızı,
24. Kaynama Noktası Bulunması
(İkili Karışım, Y = K.X)
Çözüm:
Çözüm:
26. Aşağıdaki maddelerden oluşan üçlü karışım sıvı halde bulunmaktadır. Karışımı oluşturan maddelerin karışımdaki mol kesirleri karşılarında verilmiştir. p = 30 psia basınçta bu karışımın kaynama noktasında (kabarcıklanma noktası) oluşan buhar fazının bileşimini (mol kesirlerini) bulunuz.
n-Heksan (C6) mol kesri: 30, n-Heptan (C7) mol kesri: 20, n-Oktan (C8) mol kesri: 50, p = 30 psia
Çözüm:
.............
Ek 23. Hidrokarbonların Sabit Basınçtaki K = Y/X Eğrileri
GERİ (proje çalışmaları)