Potansiyometrik ölçmelerde bir
referans elektrot, bir indikatör elektrot ve bir potansiyel ölçme düzeneğine
gereksinim vardır. İşlemde, önemli miktarda akım çekilmeksizin elektrokimyasal
hücrelerin potansiyeli ölçülür.
Potansiyometrik yöntemler iki grup
altında toplanabilir:
·
Doğrudan
Potansiyometrik Metotlar
·
Potansiyometrik
Titrasyon Metotları
Doğrudan potansiyometrik ölçmeler
bir indikatör elektrot ile yapılabilir. Yöntem basittir, örnek çözeltisine
daldırılmış indikatör bir elektrotta oluşan potansiyel aynı elektrotun standart
bir çözeltiye daldırıldığında oluşan potansiyel ile kıyaslanır; elektrotun
algılayacağı iyon özel olduğundan herhangi bir ön ayırma işlemine gerek olmaz.
Doğrudan potansiyometrik ölçmeler analitik parametrelerin sürekli ve otomatik
olarak izlenmesine de olanak verir.
Doğrudan potansiyometrik
ölçümlerin büyük kolaylıkları yanında, yöntemin yapısında bulunan zorunlu bazı
hataların da bilinmesi ve dikkate alınması gereklidir. Bunlardan en önemlisi
pek çok potansiyometrik ölçmelerde bulunan "sıvı bağlantı"
potansiyelidir. Bağlantı potansiyeli, ölçülen değerlerin doğruluğuna bir sınırlama
getirir.
Değişik bileşimlerdeki iki
elektrolit çözeltisi arasında bir bağlantı kurulduğunda , yüzeyler arasında bir
potansiyel doğar. Bu "bağlantı potansiyeli" katyon ve anyonların
çözeltilerin sınırı boyunca farklı hızlarda hareket etmeleri nedeniyle oluşan
düzensiz dağılımlarından kaynaklanır.
Şekil-1: İyonların
farklı aış hızları nedeniyle bağlantı potansiyeli oluşumu
Aşağıda
bazı sıvı bağlantı potansiyelleri (25 0C’de) verilmiştir.
Hücre diyagramı: 0.1 M NaCl I 0.1
M KCl Potansiyel: -6.4 mV
Hücre diyagramı: 0.1 M NaCl I 3.5
M KCl Potansiyel: -0.2 mV
Hücre diyagramı: 1 M NaCl I 3.5 M
KCl Potansiyel:
-1.9 mV
Hücre diyagramı: 0.1 M HCl I 0.1 M
KCl Potansiyel: +27 mV
Hücre diyagramı: 1 M HCl I 0.01 M
KCl Potansiyel:
+30 mV
Hücre diyagramı: 0.1 M HCl I 3.5 M
KCl Potansiyel: +3.1 mV
Örneğin, hücre diyagramı:
HCl (1
M) l HCl (0.01 M)
Olan bir hücrede hidrojen ve
klorür iyonları daha derişik çözeltiden daha seyreltik çözeltiye geçme
eğilimindedirler. Bu geçişteki yürütücü kuvvet konsantrasyonlar arasındaki
farkla orantılıdır. İyonların sabit bir kuvvet altındaki hareket hızları (veya
akışları) birbirinden farklıdır. Bu örnekteki hidrojen iyonunun akış hızı
klorür iyonuna göre bir kaç kez daha yüksektir. Bunun bir sonucu olarak da
difüzyon olayında hidrojen iyonu klorür iyonundan hızlı hareket eder ve onun
önüne geçer; yük dağılır (Şekil-2b). Birbiriyle bağlantıda olan iki çözeltinin
daha seyreltik olan tarafı hidrojen iyonunun bu hızlı hareketi nedeniyle
pozitif olarak yüklenirken konsantre taraf klorür iyonunun daha yavaş hareketi
sonucu negatif yük kazanır. Açığa çıkan yük iki iyonun hareketlilik farkına
engel olmak ister ve bir süre sonra denge konumuna erişilir. Bu yük dağılımı
nedeniyle oluşan bağlantı potansiyeli farkı 30 mV veya daha fazla olabilir.
Şekil-2(b)'de görüldüğü gibi basit
bir sistemde bağlantı potansiyelinin büyüklüğü, ortamdaki iki iyonun akış
hızlarından hesaplanabilir. Yine de bu hesaplar ancak çok basit hücreler için
mümkün olabilmektedir. İki çözelti arasına konsantre bir elektrolit çözeltisi
(tuz köprüsü) konması halinde sıvı bağlantı potansiyelinin önemli derecede
azaldığı deneylerle saptanmıştır. Böyle bir köprüde tuzun konsantrasyonu yüksek
ve tuzdaki iyonların akış hızları birbirine yakın olmalıdır. Doygun potasyum
klorür her iki yönden de uygun bir tuzdur; konsantrasyonu oda sıcaklığında
4M'ın üstündedir ve potasyum ve klorür iyonlarının akış hızları birbirinden
sadece %4 kadar farklıdır. Böyle bir köprü ile bağlantı potansiyeli birkaç
milivolta kadar, pek çok durumlarda ihmal edilebilir düzeye kadar düşer.
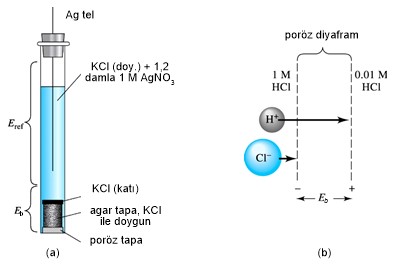
Örneğin, Şekil-2(a)’da görülen
gümüş/gümüş klorür elektrodunda,
yarı
reaksiyon: AgCl (k) ¨ Ag (k) + Cl-
iki tip potansiyel oluşumu söz
konusudur; referans elektrot potansiyeli (Eref) ve bağlantı potansiyeli
(Eb).
Şekil-2: (a) Ag/AgCl elektrodunda Eref ve Eb
potansiyellerinin oluştuğu kısımların ve, (b): Eb’yi oluşturan sıvı
bağlantısının şematik görünümleri (okların uzunluğu, iyonların relatif hızlarını gösteri)
Doğrudan potansiyometrik ölçmede
kullanılan bir hücrenin gözlenen potansiyeli Egöz, indikatör
elektrotun, referans elektrotun ve bağlantı potansiyelinin değerleri ile
belirlenir.
Egöz = Eref - Eind + Eb
Bağlantı potansiyeli Eb
iki kısımdan meydana gelir: birincisi örnek çözeltisi ile tuz köprüsünün
bağlandığı kısımda, ikincisi ise köprünün referans elektrotun olduğu çözeltiyle
bağlantı ettiği yüzeyde oluşur. Bu iki potansiyel birbirinin etkisini yok etme
eğilimindedirler, ancak bunu nadiren tam olarak yapabilirler. Denklemdeki Eb
değeri 1mV veya daha yüksek değerlere
çıkabilir.
İndikatör elektrot potansiyelinin,
seçici olduğu M+n iyonunun a1 aktivitesi ile ilişkisi
Nernst denklemine göre verilebilir.
Burada L bir sabittir. Metalik
elektrotlar için L indikatör elektrotun standart potansiyelidir, membran
elektrotlar durumunda ise L bilinmeyen, zamana bağımlı asimetri potansiyelini
de içerir.
E = L
- 0.0591 pH ve,
Egöz = Eref - Eind + Eb
denklemleri birleştirilir ve
yeniden düzenlenirse aşağıdaki eşitlikler elde edilir.
Yeni sabit K üç ayrı sabitten
oluşur, bunlardan en az biri (Eb) teorik olarak değerlendirilemeyecek
bir büyüklüktür. Bu nedenle, M'nin standart bir çözeltisi yardımıyla deneysel
olarak önce K sabiti belirlenmeli, sonra pM değeri için son denklem
kullanılmalıdır.
Elektrot kalibrasyon işleminde, denklemdeki K değeri pM'si
bilinen bir veya daha fazla standart çözeltinin Egöz değeri
ölçülerek saptanır. Sonra K’nın örnek çözeltinin ölçümü süresince değişmediği
varsayılır. Kalibrasyon, çoğunlukla, örnek çözeltinin pM'sinin tayin edildiği
anda yapılır; eğer ölçme birkaç saat gecikirse yeni bir kalibrasyon gerekli
olabilir.
Elektrot kalibrasyon yöntemi
basitlik, sürat ve pM'nin sürekli izlenmesine olanak vermesi bakımlarından
avantajlıdır. İki önemli dezavantajı vardır: analiz sonuçlarının konsantrasyon
yerine aktivitelerle verilmesi ve elde edilen analiz sonuçlarının doğruluğunun bağlantı
potansiyelinin neden olduğu hata ile sınırlandırılmış olmasıdır; ne yazık ki bu
hata tümüyle giderilememektedir.
Elektrot, çözeltideki ilgili
iyonun konsantrasyonu yerine aktivitesini algılar. Genelde ise bilim adamları
konsantrasyonla ilgilenirler ve potansiyometrik ölçmelerden konsantrasyon
miktarının saptanabilmesi için aktivite katsayısı verilerine gereksinim vardır.
Bu konuda fazla veri yoktur. Çözeltinin iyonik şiddeti bilinmiyorsa veya çok
yüksekse Debye-Hückel denklemi uygulanamayacağından aktivite katsayıları da
hesaplanamaz. Aktivite ve konsantrasyonun aynı kabul edilmesi durumunda ise,
özellikle çözelti çok değerlikli iyon içeriyorsa önemli hatalar yapılır.
Aktivite ve konsantrasyon
arasındaki fark Şekil-3’de bir örnekle gösterilmiştir. Burada alttaki noktalı eğri,
bir kalsiyum elektrotu potansiyelinin kalsiyum klorür konsantrasyonu ile
değişimini gösterir (aktivite veya konsantrasyon skalası logaritmiktir).
Eğrideki doğrusallıktan sapma elektrolitin konsantrasyonu arttıkça iyonik
kuvvetin de artmasından ileri gelir; tabii bu durumda kalsyum iyonunun aktivite
katsayısı düşer. Bu konsantrasyonlar aktivite değerlerine çevrildiğinde,
üstteki kesiksiz çizgi ile verilen eğri elde edilir; bu bir doğru şeklindedir
ve 0.296 bulunan eğimi teorik eğim ile aynıdır.
İyonik kuvvetten tek değerlikli
iyonların aktivite katsayıları çok değerlikli iyonlara göre daha az
etkilenirler. Bu nedenle Şekil-3’de görülen etki H+, Na+
ve diğer tek değerlikli iyonlar için daha zayıftır.
Potansiyometrik pH ölçmelerinde,
kalibrasyon olarak kullanılan standart tamponun pH'ı hidronyum iyonlarının
aktivitesine dayanır. Hidrojen iyonu analiz sonuçları da bu nedenle aktivite
değerleridir. Örnek çözeltinin iyonik kuvveti yüksek olursa hidrojen iyonu
konsantrasyonu ölçülen aktivite değerinden hissedilir derecede sapar.
Şekil-3: Saf kalsiyum klorürden hazırlanan değişik
konsantrasyonlardaki (ve aktivitelerdeki) çözeltilerde kalsiyum iyon elektrodu
ile okunan değerlerin konsantrasyon ve aktivite ile değişimi
b. Elektrot Kalibrasyon Yönteminde Zorunlu
Hata
Denklemde K'nın kalibrasyondan
sonra sabit kabul edilmesi örneğin hesaplanan pM’inde zorunlu hataya neden
olur; bu durum elektrot kalibrasyon yönteminde karşılaşılan önemli bir
dezavantajdır. K'nın sabit olması çok nadir, tesadüfi bir olaydır. Çünkü örnek
çözeltisinin bileşimi, kalibrasyon çözeltisinin bileşiminden daima farklıdır.
Tuz köprüsü kullanılması halinde bile K sabiti içinde bulunan bağlantı
potansiyeli değeri farklı bileşimlerdeki çözeltiler için değişik değerlerdedir.
Bu değişiklik, çoğunlukla 1 mV veya daha fazladır.
K daki 1 mV'luk değişikliğin
aktivite veya konsantrasyonda yarattığı relatif hata,
n=1
olduğunda: %4
n=2
olduğunda: %8
Bu değişiklik tuz köprüsü içeren
tüm hücrelerle yapılan ölçmelerde karşılaşılan karakteristik bir durumdur ve bu
nedenle olan hata hücre potansiyelleri ölçümünde gösterilecek titizlikle veya
çok duyar aletler kullanılmasıyla da giderilemez; hatta hatanın kaynağı olan
K'daki değişikliği tamamıyla yok edebilecek bir yöntemin tavsiye edebilmesi
bile olanaksızdır.
Potansiyometrik ölçmeleri konsantrasyon cinsinden elde etmek
için Şekil-3’deki noktalı eğride görüldüğü gibi ampirik kalibrasyon eğrileri
kullanılmalıdır. Bu yöntemin başarılı olması standardın iyonik bileşiminin
örneğinkine oldukça yakın olmasıyla sağlanabilir(kompleks örnekler için
koşullar çok karışıktır.
Elektrolit konsantrasyonlarının çok yüksek olmadığı hallerde
örnek ve kalibrasyon standardına bilinen miktarda inert bir elektrolit ilave
edilir. Bu koşullarda örnekteki eleoktrolitin elektrot potansiyeline ilave
etkisi çok az olur ve ampirik kalibrasyon eğrisi konsantrasyonu gösterir. Bu
yöntem şehir suyunda fluorürün potansiyometrik tayininde kullanılır. Bunun için
örnek ve standart, sodyum klorür, bir sitrat tamponu ve bir asetat tamponu
içeren bir çözelti ile 1/1 oranın da seyreltilir; seyreltici çözelti, örnek ve
standardın iyonik şiddetinin değişmemesi için yeteri kadar derişik olmalıdır.
Yöntem 1 ppm e kadar olan fluorür iyonunu %5 bağıl (relatif) duyarlıkla ölçmeye
olanak verir.
Standart-katma yönteminde, hacmi
bilinen bir örnekle çalışılır. Örneğin potansiyeli ölçülür, sonra örneğe az
miktarda standart ilave edilir ve tekrar potansiyel ölçülür. Burada, standart
ilavesinin çözeltinin iyonik şiddetini, dolayısıyla aktivite katsayısını
değiştirmediği varsayılır, hatta bağlantı potansiyelinin de önemli derecede
etkilemediği kabul edilir. Standart ilavesinden önce ve sonraki potansiyeller E1
ve E2 ise,
eşitliği yazılır. Burada a1
örnekteki iyonun aktivitesi, f aktivite katsayısı ve Cx molar konsantrasyonudur. Vx ml
örneğe molar konsantrasyonu Cs olan standartdan Vs ml
ilave edilmesiyle potansiyel E2 olmuştur. Bu durumda,
Buna göre Cx standardın
konsantrasyonu, standart ve örneğin hacimleri ve DE‘den kolaylıkla hesaplanabilir.
ÖRNEK
Bir doygun kalomel elektrot ve bir
kurşun iyon elektrodu bulunan bir hüreye 50.00 mL örnek konulmuştur; okunan
potansiyel -0.4706 V’dur. Aynı çözeltiye 5.00 mL 0.02000 M standart kurşun
çözeltisi ilave edildiğinde, potansiyometrede 0.4490 V değeri okunmuştur.
Örnekteki kurşunun molar konsantrasyonu nedir? Pb+2 aktivitesinin
yaklaşık olarak [Pb+2]:konsantrasyonuna eşit olduğu varsayılıyor.
Çözüm:
Cam elektrot hidrojen iyonu
tayininde kullanılan en önemli indikatör elektrotdur. pH'a karşı duyar diğer
elektrotlara göre kullanımı daha kolaydır ve ölçümü engelleyen başka iyonların
sayısı oldukça azdır.
Cam/kalomel elektrot sistemi pek
çok koşullarda pH ölçümü için başarıyla kullanılır. Kuvvetli yükseltgeyiciler,
indirgeyiciler, proteinler ve gazların bulunduğu çözeltilerde herhangi bir
engelleme olmadan pH ölçümü yapılabilir; hatta viskoz ve yarı katı sıvılarda
bile pH tayini yapılabilir.
Özel uygulamalara yönelik
elektrotlar da vardır. Bir damla veya daha az bir çözeltinin veya bir diş oyuğunun
pH'ını ölçebilecek kadar küçük elektrotlar, canlı hücrelerin pH'ını ölçebilen
mikro elektrotlar, pH'ın sürekli izlenmesini gerektiren sıvı akımlarına
yerleştirilen elektrot sistemleri ve mide asiditesini ölçmek için yutturularak
mideye daldırılan küçük cam elektrotlar, (kalomel elektrot ağızda tutulur) özel
bazı elektrotlardır.
Cam Elektrotla pH Ölçümünde
Karşılaşılan Hatalar
pH metre ve cam elektrotların
yaygın olarak kullanılması kimyacıyı her zaman doğru sonuç alındığı gibi bir
yanılgıya düşürülebilir. Oysa elektrot sistemleri için bazı sınırlamalar ve çeşitli
hata kaynakları bulunur.
1. Alkali hatası: Herhangi bir cam
elektrot pH > 9 'da alkali metal iyonlarına karşı kısmen duyar olmaya
başlar.
2. Asit hatası: pH < 0.5 ‘in
altındaki değerlerde cam elektrotlarla elde edilen sonuçlar gerçek değerlerden
bir miktar yüksektir.
3. Nem kaybetme (kuruma):
Elektrotun nemini kaybetmesi kararsız sonuçların alınmasına ve hataya neden
olur.
4. Tamponlanmış nötral
çözeltilerdeki hatalar: Zayıf olarak tamponlanmış nötrale yakın çözeltilerde
elektrot yüzeyindeki tabaka ile çözelti arasındaki denge oluşumu yavaştır.
Dengenin kurulması için gerekli zamanın (birkaç dakika) verilmemesi durumunda
hatalı ölçmeler yapılır. Zayıf tamponlanmış bölgelerde pH tayininde cam
elektrot su ile iyice çalkalanır ve örneğe daldırılır, örnek miktarı çok fazla
ise elektrot örneğin değişik kısımlarına daldırılarak kararlı bir değer elde
edilmeye çalışılır. Bu durumda iyi bir karıştırmayla örnek homojen hale
getirilir olabilir. Kararlı okuma için bir kaç dakika beklenmelidir.
5. Bağlantı potansiyelindeki
değişiklikler:Bağlantı potansiyellerindeki değişikliklerden oluşan hatalar pH
ölçümünde karşılaşılan temel bir hatadır ve herhangi bir düzeltme ile
giderilemez. 0.01 pH'dan daha güvenilir bir sonuç almak çoğunlukla
olanaksızdır. Hatta bu hata 0.03 pH'a kadar bile çıkabilir. Diğer taraftan
benzer çözeltiler arasındaki pH farkını veya bir çözeltinin pH
değişikliğini 0.001 birim duyarlıkla
ölçmek mümkündür.
6. Standart tamponun pH'ındaki
hata: Kalibrasyonda kullanılacak tamponun hatalı hazırlanması veya hazırlanmış
tamponun bekleme nedeniyle bileşiminin değişmesi (organik kısımlar bakteriler
tarafından etkilenerek tamponun zamanla
kirlenmesine neden olur) pH ölçümünde hatalı sonuçlara yol açar.
Bir potansiyometrik titrasyonun
eşdeğerlik noktası, uygun bir indikatör elektrotun potansiyeli ile saptanır.
Potansiyometrik bir titrasyonda, doğrudan potansiyometrik ölçümlere göre daha
değişik bilgiler elde edilir. Örneğin, 0.100 M asetik asit ve 0.100 M
hidroklorik asit çözeltilerinin pH'a duyar bir elektrot ile doğrudan potansiyometrik
ölçümleri çok farklı pH değerleri verir, çünkü asetik asit çözeltide kısmen
disosiye olurken hidroklorik asidin disosiyasyonu tamdır. Oysa bu iki asitin
eşit hacimlerdeki çözeltilerinin nötralizasyonu için eşit miktarlarda standart
baz harcanır.
Potansiyometrik titrasyonla dönüm
noktası tayini yöntemi, indikatörle dönüm noktası saptanmasından çok daha doğru
sonuçlar verir. Yöntem, özellikle renkli ve bulanık çözeltiler ile çalışmada ve
çözeltideki bilinen iyonların tayininde oldukça başarılıdır. Ancak indikatörle
yapılana göre daha fazla zaman alır.
Şekil-4'de potansiyometrik
titrasyon yapılabilen iki tipik sistem görülmektedir.
Şekil-4: Tipik potansiyometrik titrasyon sistemleri
Örneğin, 2.433 milieşdeğer Cl-
‘ün 0.1000 M AgNO3 ile titre edildiğini varsayalım. Titrasyonda,
titrantın her ilavesinden sonra hücre potansiyeli (veya bir pH değeri) ölçülür,
kaydedilir. Deneyin başlangıcında titrant fazla miktarlarda ilave edilir; dönüm
noktasına yaklaşılırken (bu durum her ilaveden sonra potansiyel değişimlerinin
büyümesiyle anlaşılır) ilaveler daha küçük miktarlarda yapılır.
Titrantın her ilavesinden sonra
reaksiyonun dengeye gelmesi için yeterli bir süre beklenmelidir. Çökelme
reaksiyonları için bu süre bir kaç dakika olabilir, özellikle eşdeğerlik
noktası yakınlarında dengeye ulaşma süresi uzar. Denge noktası, ölçülen
potansiyelin bir kaç milivolttan daha fazla değişmediği potansiyel olarak
alınır. İyi bir karıştırma, denge noktasına gelme sürecini kısaltır. Potansiyometrik
veriler Tablo-1’de toplanmıştır.
Tablo-1: 2.422 mmol Klorür İyonunun 0.1000 M AgNO3 ile
Potansiyometrik Titrasyon Verileri(*)
Potansiyometrik Titrasyon Verileri(*)
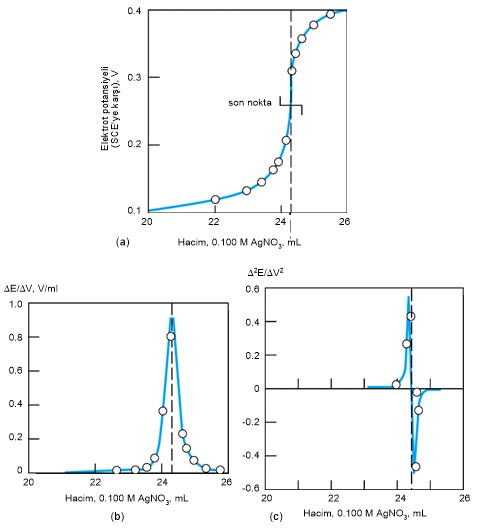
Potansiyometrik bir titrasyonun
dönüm noktasının tayininde bir kaç yöntem uygulanabilir. En çok uygulanan
yöntem potansiyel değerlerinin harcanan titrant hacmine göre doğrudan grafiğe
geçirilmesidir (Şekil-5a). Eğrinin dik olarak yükselen bölgesinin ortası dönüm
noktasıdır.
Tablo-1’in 3. kolondaki veriler
titrantın birim değişimine karşı potansiyeldeki değişimlerini (DE/DV)
gösterir. Bu parametrenin ortalama hacme karşı grafiğe alınmasıyla dönüm
noktasının keskin bir maksimumda bulunduğu bir eğri elde edilir (Şekil-5b). DE/DV
değerleri hesapla bulunabilir veya titrasyon sırasında doğrudan cihazdan
okunabilir (potansiyel yerine). Tablodaki değerlerde maksimum nokta 24.3 ve
24.4 ml arasındadır; dönüm noktası için
24.35 ml en uygun hacimdir.
Şekil-5(c), ikinci türev
eğrisidir; D2E/DV2.
İkinci türev eğrileri tablodaki derğerlerden kolaylıkla çizilebilir. Bu amaçla
kullanılan otomatik titratörler vardır. Elektrotdan alınan ve yükseltilen
sinyal indikatör elektrotun potansiyelinin ikinci türevi ile orantılı bir
voltaja dönüştürülür. Alınan verilerle Şekil-5(c)'de görüldüğü gibi bir grafik
elde edilir; eşdeğerlik noktasında sinyalin işareti değişir. İşaretin değişmesi
titrant akışını sağlayan vana sistemini kapatır ve akış durur.
Şekil-5: 2.433 milieşdeğer Cl- ‘ün 0.1000 M AgNO3
ile titrasyonunda, (a) potansiyelin madde hacmine göre değişim, (b) birinci türev, ve (c) ikinci türev eğrisi
Kimyasal reaksiyonda birbiriyle reaksiyona giren maddelerin eşdeğer molar oranlarda olması ve elektrot reaksiyonlarının da geri dönüşümlü reaksiyonlar olması koşullarında bu varsayım doğrudur. Bu koşulların karşılanamaması durumunda elde edilen eğri asimetrik olur (Şekil-6, B eğrisi). Demir(2)'nin ceryum(4) ile yükseltgenmesinde elde edilen eğri ise eşdeğerlik noktası yakınlarında simetriktir. Diğer taraftan her mol permanganat için 5 mol demir(2) harcanır ve simetrisi çok bozuk bir eğri elde edilir.
Eşdeğerlik noktasının bulunduğu
bölge içinde bu eğrilerin potansiyel değişimi çok yüksektir ve dönüm noktası
olarak eğrilerin dik olarak yükselen kısmının tam ortası alınırsa normal
çalışmalarda fazla bir hata yapılmamış olur. Ancak özel bir hassasiyet
isteniyorsa veya çok seyreltik çözeltilerle çalışılıyorsa dönüm noktası saptanmasında
eğrinin simetriden sapma faktörü dikkate alınmalıdır. Bu gibi hallerde bir
standartın titrasyonu yapılarak düzeltme saptanır; veya eşdedeğerlik noktasının
doğru yeri teorik olarak hesaplanabilir.
Şekil-6: 100 ml 0.100 N Fe+2 çözeltisinin, (A) Ce+4
ve (B) MnO4- ile
titrasyon eğrileri
Gran, titrasyon süresince elde
edilen değerlerden sadece reaksiyonun tamamlanmasına yakın olanların
kullanılmasıyla dönüm noktasının bulunmasını sağlayan bir yöntem
geliştirmiştir. Yöntem, normal dönüm noktası saptama yöntemlerine göre daha az
veriye dayandığından avantajlıdır. Hatta eşdeğerlik bölgesinde p
fonksiyonundaki değişiklik hızı küçük olduğundan elde edilen dönüm noktası daha
doğru olur.
Bir örnek olarak klorür
iyonlarının gümüş nitrat ile titrasyonu için Tablo-1'de toplanan verilerin Gran
yöntemi ile değerlendirmesini yapalım. Bu titrasyonda eşdeğerlik noktasından az
önce gümüş elektrot klorür iyonlarına karşı ikinci-dereceden bir elektrot gibi
davranır ve hücre potansiyeli Egöz , aşağıdaki eşitlikle tarif
edilir.
Egöz
= E0AgCl - 0.0591 log [Cl-] - ESKE
Bağlantı potansiyeli,
potansiyometrik titrasyonda önemli olmadığından ihmal edilmiştir. Denklem,
denklemiyle verilir. Burada VCl
ve VAg örnek ve titrant çözeltilerinin ölçülen hacimleri, NCl
ve NAg de iki çözeltinin başlangıç konsantrasyonlarıdır. İki
eşitliğin birleştirilmesi ve yeniden düzenlenmesiyle aşağıdaki eşitlik elde
edilir.
(VCl
NCl – VAg NAg) = (VCl +VAg)
antilog (-16.9 Egöz + K’)
Bir titrasyonda bu eşitlikteki VAg
ve Egöz dışındaki bütün terimler sabittir. Buna göre (VCl
+ VAg) antilog(-16.9 Egöz) nün VAg karşı çizilen
grafiği bir doğru olur. Ayrıca eşdeğerlik noktasında denklemin sol tarafı
sıfırdır. Bu nedenlerle, antilog eksenindeki doğrunun sıfıra ekstrapolasyonu
eşdeğerlik-noktasındaki hacmi verir.
Şekil-7: Tablo-1’deki verilerin Gran eğrisi
Tablo-1'deki
verilerle çizilen gran eğrisi Şekil-7'de görülmektedir. İlk dört nokta düzgün
bir doğru verir. Bundan sonraki noktalar doğrusallıktan sapmıştır; sapma
eşdeğerlikten 2 ml kadar önce başlamıştır. Tamamlanma derecesi daha az olan
reaksiyonlarda doğrunun eğilmesi daha önce başlar. Bu yöntemle eşdeğerlik noktası
Tablo-1'deki 19 veri yerine 3 veya 4 veri ile sağlıklı olarak saptanabilir.
Dönüm noktası
tayinini belirlenmiş bir potansiyele kadar titrasyon yöntemiyle de yapılabilir. Bir yöntemde dönüm noktası
potansiyelinin önceden saptanması ve titrasyonun belirlenen bu potansiyele
kadar yapılmasıdır. Seçilen değer normal potansiyellerden hesaplanan teorik
eşdeğerlik potansiyeli veya standart çözeltilerin titrasyonu ile saptanmış olan
ampirik bir potansiyeldir. Bu yöntemde sistemin eşdeğerlik-noktası kararlı
olmalıdır.
Çöktürme titrasyonlarında
kullanılan indikatör elektrotu çoğunlukla, reaksiyona giren katyonun metalidir;
örneğin AgNO4 ile Cl- tayini yapılıyorsa Ag indikatör
elektrot kullanılır.
Titrasyon işlemindeki iyonlardan
herhangi birine karşı duyar olan membran elektrotlar da indikatör elektrot
olarak kullanılabilirler. İnert bir platin elektrot da bu amaçla
kullanıldığında bir indikatör elektrot gibi davranır.
Örneğin, ferrisiyanür iyonlarının
bulunduğu bir ortamda çinko iyonunun ferrosiyanür iyonları ile titrasyonu bir
platin elektrotla izlenebilir. Elektrotda,
Fe(CN)
6-3 + e- ¨
Fe(CN)6-4
yarı-reaksiyonun belirlediği bir
potansiyel vardır. Titrasyon boyunca çinko iyonları ferrosiyanür ile reaksiyona
girer ve potansiyelde önemli bir artış olmaz. Dönüm noktasına ulaşıldığında
titrantın fazlası ortamdaki ferrosiyanür konsantrasyonunu süratle artırır,
dolayısıyla elektrot potansiyeli uygun miktarda değişir.
Halojenler, halojenoidler,
merkaptanlar, sülfürler, arsenatlar, fosfatlar ve okzalatların tayininde
kullanılan gümüş nitrat uygulama sahası çok geniş olan bir volumetrik çöktürme
maddesidir. Bu tip tayinlerin hepsinde gümüş indikatör elektrotu kullanılır.
Referans elektrot olarak
çoğunlukla kalomel elektrot seçilir. Ancak çok seyreltik çözeltilerle
çalışıldığında veya çok yüksek duyarlık istendiğinde Şekilde görülen tipte bir
kalomel elektrot, poröz diskten (tuz köprüsü) çözeltiye klorür iyonları sızıntısı
olacağından uygun değildir. Sorunu gidermek için kalomel elektrot derişik
potasyum nitrat çözeltisine içine daldırılır, bu çözelti de %3 kadar potasyum
nitrat içeren bir agar köprüsüyle örnek çözelti ile bağlanır. Titrant ve örnek
çözeltilerin konsantrasyonlarının 0.1N veya daha fazla olması durumunda Şekildeki
kalomel elektrot doğrudan kullanılabilir ve önemli bir hataya da neden olmaz.
Gümüş/doygun kalomel elektrot
sistemi ile klorür, bromür ve iyodür iyonlarının verdiği teorik titrasyon
eğrileri Şekil-9'da görülmektedir. Sol taraftaki ordinat volt olarak hücre
potansiyellerini,sağ taraftaki de pAg'ü gösterir. Noktalı eğriler iyodür
iyonunun deneysel verileriyle çizilen eğrilerdir; bunlar teorik değerlerden
katı yüzeyinde adsorbsiyon etkisi nedeniyle bir dereceye kadar farklıdır.
Eşdeğerlik noktasından hemen önce iyodür iyonları katı yüzeyinde tutulurlar ve
böylece çözeltideki iyodür iyonları konsantrasyonu düşer,potansiyel bir miktar
yükselir. Eşdeğerlikten sonra ise adsorbsiyon gümüş iyonları konsantrasyonunu
azaltıcı yöndedir; potansiyel değerleri azalır. Bu etki klorür ve bromür
iyonları için çok zayıftır.
Eşdeğerlik-noktasının bulunduğu
bölgede, elektrot potansiyelindeki değişiklik reaksiyon ürünlerinin çözünürlüğü
azaldıkça artar (Şekil-9). Böyle bir etki tamamlanma derecesi çok yüksek olan
reaksiyonlarda da görülür; bu durum birinciye göre daha geneldir ve kompleks oluşumu,
nötralizasyon, yükseltgenme-indirgenme reaksiyonlarında karşılaşılır.
Şekil-9'de saptanan bir başka
gözlem de farklı iki konsantrasyondaki klorür çözeltileri için elde edilen
eğrilerin durumudur; örnek ve titrant çözeltilerinin konsantrasyonları azaldıkça
dönüm noktasının keskinliği(veya belirginliği) de azalır. 0.001N kadar
seyreltik bir klorür çözeltisinin titrasyonu yapıldığında relatif hata %1
civarında olur. Oysa ve bromür iyodür çözeltileri daha da düşük konsantrasyonlarda
bile başarılı sonuçlar verir, çünkü bu iyonların gümüş iyonu ile reaksiyonlarının
tamamlanma dereceleri daha yüksektir.
Aşağıda bu eğrilerin elde
edilişini açıklayan bir örnek verilmiştir. Şekildeki noktalı eğriler sodyum
iyodür için I- ve Ag+ iyonlarının AgI çökeleği üzerindeki adsorbsiyonları
nedeniyle deneysel verilerin teorik eğriden sapmalarını gösterir.
Bir gümüş indikatör elektrotu ve
bir doygun kalomel elektrotdan oluşan elektrot sistemi ile, 100 ml 0.0200 M
sodyum iyodürün 0.100 M gümüş nitrat ile potansiyometrik titrasyonu yapılıyor.
a. Eşdeğerlik noktasından 1.00 ml
önceki hücre potansiyeli nedir?
b. Eşdeğerlik noktasındaki hücre
potansiyeli nedir?
c. Eşdeğerlik noktasından 1.00 ml
sonraki hücre potansiyeli nedir?
Gerekli elektrot potansiyeli
verileri aşağıda verilmiştir.
Ag I
(k) +e- ¨ Ag (k)+ I- E0 = - 0.151V
Hg2Cl2
(k) ¨ 2 Hg (s)+ 2 Cl-
(doygun KCl) E0 = +0.241V
a. Tirasyonda 20.0 ml AgNO3
'a gereksinim vardır. 19.0 ml titrant ilave edildikten sonra iyodürün normal
konsantrasyonu,
olur. Çökeleğin çözünürlüğünden
ilave bir miktar daha iyodür oluşur. Bu nedenle oluşan iyodürün konsantrasyonu
gümüş iyonları konsantrasyonuna eşit olacaktır, böylece toplam iyodür
konsantrasyonu,
[ I-
]toplam = 8.40 x 10-4 + [Ag+]
olur. [Ag+] <<
8.40 x 10-4 M olduğu varsayılabilir, böylece indikatör elektrotun potansiyeli
hesaplanır.
EAg
= - 0.151- 0.0591 log 8.40 x 10-4
EAg
= 0.031V
Kalomel elektrot anod ise, hücre
potansiyeli bulunur.
Ehücre
= 0.131- 0.241 = - 0.210V
b. Eşdeğerlik noktasında:
[Ag+]
= [ I- ]
Gümüş iyodürün çözünürlük çarpımı
8.3 x 10-17 dir.
Elektrotların polaritelerinin, titrantın
ilk ilavesi ile eşdeğerlik noktası arasında değiştiğini belirtmek gerekir.
Ancak böyle bir durumla çok sık karşılaşılmaz.
c. Eşdeğerlik noktası 1.00 ml
geçildiğinde fazla Ag+ konsantrasyonu:
Potansiyometrik yöntemin önemli
bir avantajı bir titrantla reaksiyon veren ve bir karışım halinde bulunan
maddelerin çoğu zaman ayrı ayrı tayinine olanak vermesidir. Şekil-10'da eşdeğer
molaritede iyodür, bromür ve klorür iyonlarının bulunduğu bir karışımının
titrasyon eğrisi verilmiştir.Titrasyonun başlangıcında çözünürlüğü en düşük
halid olan gümüş iyodür çöker. Teorik olarak hesaplandığında çözeltide bulunan
iyodür iyonlarının %0.02 ‘si gümüş iyodür olarak çökeldikten sonra bromür
iyonlarının çökelmesi de başlar.
Ancak ilk çökelen gümüş iyodür
olduğundan iyodür iyonunun tamamı çökelinceye kadar eğrinin şekli Şekil-9'da
görülen gümüş iyodür çökelme eğrisinin şekline benzer. Sonra gümüş bromür
çökelir; burada da teorik olarak bromür iyonlarının %0.3 kadarı çökelinceye
kadar gümüş klorür çökelmesi olmaz. Bu nedenle titrasyon eğrisi bu bölgede
sadece bromür iyonunun çökelme eğrisinin şekline benzer. Son olarak klorürün
çökelmesi başlar, eğrinin son kısmı Şekil-9'daki klorür iyonunun çökelme
eğrisiyle aynı görünümü alır.
Halojenür karışımlarının tek bir
potansiyometrik titrasyonla tayin edilebileceği Şekil-10’da gösterilmiştir;
gerçekte böyle bir analizin yapılabilirliği deneysel olarak da ispatlanmıştır.
Şekil-10: 2.50 mmol g I-, Br- ve Cl-
‘ün 0.2 M AgNO3 ile potansiyometrik titrasyonu
Bu üç iyondan
herhangi ikisinin bulunduğu bir karışımın titrasyonunda, birinci dönüm
noktasına ulaşmak için harcanan gümüş nitrat çözeltisi miktarının teorik olarak
gerekli miktardan biraz daha fazla olduğu, ancak toplam hacmin ise teorik değere
eşit olduğu saptanmıştır.
Bu gözlemler, az
çözünen gümüş halojenürün çökmesi sırasında, ona kıyasla çözünürlüğü daha fazla
olan diğer halojenürün de kısmen beraber çökmesiyle açıklanır, böylece
titrasyonun birinci kısmında gereğinden fazla titrant harcanır.
Beraber çökelme
hatasına rağmen potansiyometrik titrasyon halojenür karışımlarının
analizlerinde kullanılan yararlı bir yöntemdir. Eşit miktarlardaki halojen iyonlarının
analizinde yapılan relatif hata %1- 2 arasındadır.
Çözünebilen komplekslerin oluşum
reaksiyonlarında dönüm noktası tayininde metal ve membran elektrotlardan
yararlanılabilir. Kompleksometrik titrasyonda kullanılan en önemli madde bir
amino karboksilik asitler grubu olan etilen-diamintetraasetik asittir (EDTA) ve
H4Y formülü ile tanımlanır; yapısı aşağıdaki gibi gösterilebilir.
İki amin azotu ve dört karboksilat
fonksiyonel grubu metal iyonları ile bağ oluşumunu sağlar. Katyonun yükü
dikkate alınmayarak kompleks oluşum reaksiyonu aşağıdaki gibi yazılabilir.
M+n
+ H4Y ¨ M Y(n-4) + 4 H+
Bu yöntemle yapılan analizlerden,
sert suda kalsiyum ve magnezyum tayini önemli bir örnektir. Kalsiyum
tayinindeki reaksiyon aşağıda verildiği şekildedir.
Ca+2+
H4Y ¾® Ca Y-2
+ 4 H+
EDTA anyonu için ikinci- derece
elektrot olarak civa elektrotu kullanılabilir.
Reilley ve arkadaşları civa
elektrot ile 29 adet iki, üç ve dört değerlikli iyonların EDTA titrasyonunu,
deneysel ve teorik bazda sistematik olarak incelenmişlerdir. Çalışmalarda 5-500
mg katyon, 0.05 veya 0.005N EDTA çözeltisi kullanılmıştır. Her titrasyonda
birer damla 10-3 N HgY-2 çözeltisi bulunur.
Şekil-11'de bizmut, kadmiyum ve
kalsiyum iyonları karışımı için yapılan çalışmanın eğrileri verilmiştir. Önce
pH =1.2'de bizmut(3) titre edilmiştir. Bu kadar asidik bir ortamda kadmiyum ve
kalsyum reaksiyon vermez;
M+n
+ H4Y ¨ M Y(n-4) + 4 H+
denkleminde bu iki iyon için denge
sol tarafa doğrudur.
Oysa bizmut kararlı bir kompleks
oluşturur. Bizmutun titrasyonu tamamlandıktan sonra çözeltiye asetik
asit/asetat tamponu ilave edilir ve pH = 4 yapılır, kadmiyumun dönüm noktasına
ulaşılıncaya kadar titrasyona devam edilir. Bu ortamda kalsiyum iyonları reaksiyon
vermez. Çözeltiye amonyak/amonyum klorür tamponu ilave edilerek ortam
bazikleştirilir ve sonra kalsiyum iyonlarının titrasyonu yapılır.
Şekil-11: Üç katyon karışımının potansiyometrik EDTA titrasyonu
Potansiyometrik asit-baz
titrasyonlarında cam/kalomel elektrot kullanılır. Bu yöntemde renkli veya
bulanık çözeltilerle de başarılı sonuçlar alınır.
Nötralizasyon:
HCl + NaOH
® NaCl + H2O
Şekil-12: Kuvvetli asit-baz titrasyonları; (a) NaOH’in HCl
ile, (b) HCl’in NaOH ile titrasyon eğrileri (50.00 mL örneklerle çalışılmıştır)
Kuvvetli Bir Asitin Kuvvetli Bir Baz ile Titrasyonununda
pH Değişimi
pH Değişimi
Şekil-13(a)'da disosiyasyon
sabitleri farklı olan bazı asitlerin standart sodyum hidroksit ile titre
edilmesi halinde elde edilecek teorik eğriler çizilmiştir. Şekil-131(b)’de de
bu asitlerden birisi alınarak titrasyon eğrisine örnek çözeltisinin ve
titrantın konsantrasyonlarının etkisi incelenmiştir.
Cam/kalomel elektrot sistemi ile
elde edilen deneysel eğriler bu teorik sonuçlara oldukça yakın değerler verir.
Asidin kuvveti azaldıkça ve konsantrasyonu düştükçe, dönüm noktasının
saptanması zorlaşır. Zayıf bir asitin kuvvetli bir baz ile potansiyometrik
titrasyonunun % 1'lik bağıl hata ile yapılabilmesi için, NNaA Ka
³ 10-5
olması gerektiği ileri sürülmüştür. Burada NNaA, titre edilen asitin
sodyum tuzunun dönüm noktası konsantrasyonu, Ka asitin ayrışma
sabitidir. Zayıf bazik çözeltilerin kuvvetli asitlerle titrasyonunda da benzer
yorumlar geçerlidir.
Şekil-13: (a) Titrasyon eğrilerine asit kuvvetinin
(disosiyasyon sabiti) etkisi (her eğri 50.00 mL 0.1000 M asitin 0.1000 M baz
ile titrasyonunu gösterir), (b): asetik asitin NaOH ile titrasyon eğrileri
Zayıf Bir Asitin Kuvvetli Bir Baz ile Titrasyonununda
pH Değişimi
pH Değişimi
Potansiyometrik titrasyonlar asit
karışımlarının (veya baz) titrasyonunda da başarıyla kullanılır. Karışımdaki
asitlerin disosiyasyon sabitleri birbirinden yeteri kadar farklı ise her
birinin konsantrasyonunu saptamak mümkün olur. Bu uygulamaya bir örnek Şekil-14‘de
görülen eğridir. Trikloroasetik asit ve asetik asit konsantrasyonları,
karışımın potansiyometrik titrasyon eğrisinden hesaplanabilir. İyodoasetik asit
ve asetik asit karışımı için durum farklıdır; bu iki asitin asitlik kuvvetleri
birbirinden yeteri kadar farklı olmadığından karışımın titrasyonu ile sadece
toplam asit konsantrasyonu bulunur. İki asit (veya baz) karışımındaki asitlerin
disasiyon sabitleri arasındaki oran 10-4 veya daha büyük olursa her
bir asitin konsantrasyonunu titrasyon eğrisinden bulunabilir.
Şekil-15'de çok bilinen üç
asitin titrasyon eğrileri verilmiştir;
bunların birden fazla titre edilebilir hidrojenleri vardır. Sülfürik asit (C),
iki protonun ayrışma derecesi birbirinden yeteri kadar farklı olmadığından bir
tane dönüm noktası gösterir (ikinci proton için Ka = 1.2 x 10-2
iken birinci proton tamamiyle ayrışır). Okzalik asitin K1 ve K2
arasındaki oran 1000 dir; titrayon eğrisi (B) birinci eşdeğerlik noktasında bir
eğilme gösterir. Ancak dönüm noktasının doğru olarak saptanması için gerekli pH
değişikliği değeri oldukça küçüktür; ikinci dönüm noktası çok belirgindir ve bu
asitin kantitatif tayininde bu nokta kullanılır.
Fosforik asit için K1/K2
= 105 tir; iki iyi dönüm noktası elde edilir. Bu nedenle fosforik
asit, sodyum dihidrojen fosfat ve bunların karışımının analizleri tek bir
potansiyometrik titrasyonla bulunabilir. Fosforik asitin üçüncü hidrojeninin
ayrışması çok yavaştır (K3 = 4.2 x 10-13) ve bir dönüm
noktası vermez.
Şekil-15: Polibazik asitlerin 0.100 N NaOH çözeltisi ile titrasyon
eğrileri
Asitlerin (veya Bazların) İyonlaşma Sabitlerinin Tayini
Zayıf bir asit veya bazın
iyonlaşma sabiti için potansiyometrik titrasyon eğrilerinden yaklaşık sayısal
bir değer bulunabilir. Teorik olarak bu değer, eğri boyunca bulunan noktalardan
herhangi biri kullanılarak hesaplanabilir; pratikte nötralleşmenin yarısına
gelindiği noktadaki pH değerinden yararlanılır. Örneğin, zayıf bir asit olan HA
nın titrasyonunda orta noktada,
[HA] = [A-]
olduğu varsayılır, bu durumda,
pKa = pH
Bu yöntemle saptanan bir iyonlaşma
sabiti, herhangi bir iyonlaşma sabitleri tablosunda bulunan değerden farklıdır
(2 veya daha yüksek bir faktör kadar). Çünkü iyonlaşma sabitleri tablosundaki
değerler aktivite bazına göre hesaplanmıştır, burada ise konsantrasyon
değerleri kullanılır. İyonlaşma sabitinin, daha doğru şekli olan aktivite
değerleri ile yazılmasıyla aşağıdaki K a
ifadesi çıkarılır.
Yani gerçek pKa
deneysel pKa 'dan aktivitelerin oranının logaritması kadar farklıdır.
Titrasyon sırasında iyonik kuvvet genelde 0.1 veya daha büyüktür. Bu nedenle fA-
'nin fHA 'ya oranı HA yüksüz ise en az 0.75 olur. H2PO4-
ve HPO4-2 gibi iyonlar için bu oran daha da büyüktür.
Sulu çözgenlerdeki asit-baz
titrasyonları asidik veya bazik denge sabitlerinin 10-9 'dan büyük
olması halinde uygulanabilir. Daha zayıf asitler ve bazlar için reaksiyonun
tamamlanma derecesi eşdeğerlik noktasında yeterli pH değişikliği elde
edilmesine olanak vermeyecek kadar düşüktür. Bu gibi hallerde su yerine susuz
çözücülerin kullanılmasıyla uygun sonuçlar alınabilir. Örneğin, anilinin sulu
çözeltisi (Kb » 10-10)
çok zayıf bazik özellik gösterir ve perklorik asitle yapılan titrasyonu
başarısız olur.
Oysa anilinin glacial asitik
asitteki çözeltisinin perklorik asitle titrasyonunda anilin ve perklorik asit
arasındaki reaksiyon hemen hemen tamdır ve eşdeğerlik noktasındaki pH
değişikliği oldukca büyüktür. Benzer şekilde, fenolün (Ka » 10-10) metil izobutil keton gibi susuz bir
çözücüdeki baz ile titrasyonunda olumlu sonuç alındığı halde sulu çözeltisinde
başarısız olur.
Potansiyometrik titrasyon, susuz çözücülerdeki
titrasyonların eşdeğerlik noktalarını saptamada özellikle uygulanan bir
yöntemdir. Elektrotlar bilinen cam/kalomel elektrot sistemidir, titrasyondan
önce elektrotlar su içinde tutularak camın kuruması ve tuz köprüsündeki
potasyum klorürün çökmesi önlenir. Ölçmelerde potansiyometrenin pH skalası
yerine milivolt skalası kullanılır. Çünkü susuz çözeltilerin potansiyelleri
pH'a göre daha sağlıklı ölçülür. Ayrıca sulu tamponlar susuz ortamlarda yeterli
hassasiyet göstermezler. Bu nedenle titrasyon eğrileri ampiriktir.
Pek çok yükseltgenme-indirgenme
reaksiyon sisteminin potansiyeli platin elektrot ile ölçülür. Ölçülen
potansiyel reaksiyona giren ve reaksiyondan çıkan maddelerin konsantrasyonları
arasındaki orana bağlıdır. Pt elektrot titrasyon süresince yükseltgenme-indirgenme
sistemlerine karşı hassastır.
Demir(2)'nin standart KMnO4
çözeltisi ile titrasyonu.
Reaksiyonlar:
MnO4-
+ 8 H+ + 5e- ¨ Mn+2
+ 4 H2O E0 = 1.51
V
Fe+3
+ e- ¨ Fe+2 E0 =
0.171 V
Titrantın her ilavesinden sonra
reaksiyon olur, bu işlem iki yarı-reaksiyonun potansiyellerinin birbirine eşit
olduğu madde konsantrasyonlarına ulaşılıncaya kadar devam eder. Dengede,
Ölçülen potansiyel iki yarı-hücre
sisteminin herhangi birinden oluşan potansiyel olarak düşünülebilir.
Yükseltgenme-indirgenme
titrasyonun eşdeğerlik noktası bölgesindeki elektrot potansiyeli değişikliği
reaksiyonun tamamlanma derecesi arttıkça daha büyük olur. Diğer reaksiyon
tiplerinde de benzer etkinin olduğu görülmüştür.
Şekil-16'da standart potansiyeli
0.2 V kabul edilen hayali bir örnek çözeltinin, standart potansiyelleri 0.4
V'dan 1.2 V'a kadar değişen çeşitli titrantlarla yapılan titrasyon eğrileri
çizilmiştir, reaksiyonların denge sabitleri 2 x 103 'den 9 x 1016
'ya kadar değişmektedir. Burada, reaksiyonun tamamlanma derecesi arttıkça dönüm
noktası bölgesindeki elektrot potansiyeli değişikliğinin de arttığı açık bir
şekilde görülür.Eğriler yükseltgenme ve indirgenmede bir-elektron değişimi
olduğu varsayımına göre çizilmiştir; eğer iki-elektron değişimi olsaydı
24.9-25.1 ml titrant harcanan bölgedeki potansiyel değişimi 0.14V kadar daha
fazla bulunurdu.
Şekil-16: 50 ml 0.0500 N A çözeltisinin titrasyonu; titrant (R) ve
analitin (A) bir elektron değiştirdiği varsayılmıştır
İki yükseltgeyici veya iki indirgeyici maddenin bulunduğu
çözeltilerde iki dönüm noktası olan titrasyon eğrileri elde edilir; ancak iki
maddenin standart potansiyelleri birbirinden yeteri kadar farklı olmalıdır. Her
iki maddenin ayrı ayrı dönüm noktalarını saptamak için bu farkın en az 0.2V
olması gerekir. Bu durum, denge sabitleri birbirinden farklı iki asit
karışımının veya çözünürlükleri farklı iki iyon karışımının titrasyonuna
benzer.
100.0 mL 0.0500 M Fe+2
çözeltisinin, perklorik asitte, 0.100 M Ce+4 ile titrasyonunu
inceleyelim.
Titrasyon reaksiyonu:
Ce+4
+ Fe+2 ® Ce+3 + Fe+3
Hücre diyagramı:
Hg (s)
| 1/2 Hg2Cl2 (k) | Cl- (sulu) | | Fe+3
(sulu), Fe+2 (sulu) | Pt (k)
Hg (s)
| 1/2 Hg2Cl2 (k) | Cl- (sulu) | | Ce+4
(sulu), Ce+3 (sulu) | Pt (k)
Hg I Hg2Cl2 I Cl– II Ce+4 , Ce+3 , Fe+3,
Fe+2 I Pt
Standart kalomel elektrotta
reaksiyon:
2 Hg
(s) + 2 Cl– (sulu) ¬® Hg2Cl2 (k) + e–
E0 = 0.241 V
Pt elektrotta reaksiyonlar:
Fe+3
+ e- ¨ Fe+2 E0 = 0.767 V (1M HClO4
de)
Ce+4
+ e- ¨ Ce+2 E0 = 1.70 V (1M HClO4
de)
Hücre reaksiyonu:
2 Fe+3
+ 2Hg (s) + 2 ClР¨ 2 Fe+2
+ Hg2Cl2 (k)
2 Ce+4 + 2Hg (s) + 2 ClР¨ 2 Ce+3 + Hg2Cl2
(k)
ECe = EFe = Eçözelti
Ehücre= Ekatot – Eanot
= Eçözelti – ESCE
E0hücre = 0.767 – (0.241) = 0.526 V
Reaksiyonun
denge sabiti:
Şekil-18: 100 mL 0.050 M Fe+2 çözeltisinin 1 M
HClO4’de 0.100 M Ce+4 ile titrasyonu için teorik
titrasyon eğrisi
1. Eşdeğerlik noktasından önce
Kalan Fe+2 miktarı =
başlangıçtaki Fe+2 – ilave edile Ce+4 (~ kullanılan Fe+2
oluşan Fe+3 =
kullanılan Fe+2
3. Eşdeğerlik noktasından sonra
Aşağıda, 50.00 mL 0.05000 M Fe+2.çözeltisinin ve 50.00 mL 0.02500 M U+4.çözeltisinin titrasyon verileri ve titrasyon eğrileri aşağıda gösterilmiştir.
0.1000 M Ce+4 ile Titrasyonda Elektrot Potansiyeli (SHE’a
karşı)
Şekil-19: 0.1000M Ce+4 çözeltinin titrasyon
eğrileri; A: 50.00 mL 0.05000 M Fe+2.çözeltisi, B: 50.00 mL 0.02500
M U+4.çözeltisi
Potansiyometrik titrasyon
verilerinden E'nin V 'ye karşı türevleri alınarak çizilen eğrinin eşdeğerlik
noktasında keskin bir maksimum verdiği daha önce görülmüştü (Şekil-5b).
Diferensiyal bir titrasyonda birbirinin aynı olan iki indikatör elektrota
gereksinim vardır. Şekil-20'de tipik bir sistem görülmektedir. Burada
elektrotlardan birisi, yan bağlantısında bir lastik puar bulunan bir test
tüpünün içine konmuştur. Tüpün tabanında küçük bir delik (»1mm ) vardır ve örnek çözelti bu delikten tüpe dolarak
elektrot ile bağlantı eder.
Şekil-20: Diferensiyal potansiyometrik titrasyon sistemi
Elektrotlar birbirinin aynı
olduğundan başlangıçta her ikisinin potansiyeli de aynıdır ve potansiyel farkı
(DE) sıfırdır. Çözeltiye titrant ilave edildiğinde, tüp
içindeki elektrot yeni potansiyeli hemen algılayamaz ve hala başlangıç
potansiyelini gösterirken diğer elektrotun potansiyeli değişir; yani çözelti
bileşimindeki değişiklik elektrotlar arasında DE kadar potansiyel
farkına neden olur. Titrantın her ilavesinden sonra elektrotun bulunduğu
tüpteki çözelti, lastik puar bir kaç kez sıkılarak dipteki delikten örnek
çözelti içine boşaltılır ve ana çözeltinin homogen hale gelmesi sağlanır.
Homogenlik, iki elektrotun potansiyellerinin aynı değere gelmesiyle, yani DE = 0
olmasıyla anlaşılır. Sonra homogen çözelti tekrar tüpe dolar. Tüpte bulunan ve
elektrotu saran çözeltinin hacmi 1-5 ml gibi az miktarlarda ise titrasyonun
sonun da ilave edilen ve bu miktar ile bağlantı edemeyecek olan titrantdan
ileri gelecek hata ihmal edilebilir düzeydedir.
Potansiyometrik ilkelere göre
çalışan çeşitli otomatik titrasyon cihazları vardır. Bu tip enstrumanlar rutin
analizler için çok yararlıdır. Otomatik titratörler, el ile çalışan
potansiyometrik tekniklere göre daha hassas sonuç vermezler; ancak daha az
zaman harcandığından ekonomik yönden önemli avantajları vardır.
Titrant
Akışının Kontrolü ve Hacminin Ölçülmesi
Bir titrantın ilavesini otomatik
olarak kontrol eden ve hacmini ölçebilen çeşitli yöntemler vardır. Bunlardan en
basitinde musluk kısmı yerinde elektromagnetik bir sıkıştırma sistemi bulunan
alelade bir büret kullanılır. Büretin iç kısmında (beden-uç arası) esnek
plastik bir tüp bulunur. Titrantın akmasını önlemek için tüp yumuşak bir demir
parçası ve metal bir takoz arasında yaylı bir sistemle sıkıştırılır. Titrantı
akıtmak için de sıkıştırma sistemini saran selenoidden elektrik akımı
geçirilir. Başka bir vana sisteminde ise bir cam veya plastik tüp içine küçük
bir demir parçası konulur ve tüp ergitilerek kapatılır; parça bir büretin
içine, iki yüzeyi tapa görevi yapacak şekilde yerleştirilir. Bir selenoide akım
verildiğinde tapa açılır ve titrant akar. En çok kullanılan otomatik titrant
akışı sağlayan sistem, motor-sürücü mikrometrik bir vida ile çalışan kalibre
edilmiş bir şırıngadır.
Kalibre edilmiş bir potansiyometre
ile elektrotlara önceden bilinen dönüm noktası potansiyeli uygulanır. Bu
potansiyel ile elektrotların potansiyelleri arasında bir farklılık olduğunda
"hata" sinyali alınır. Sinyal büyütülür ve büretin selenoidle çalışan
vanasından elektrik akımı geçmesini sağlayan elektronik düğmeyi kapatır. Hata
sinyali sıfıra yaklaşırken selenoiddeki akım kesilir ve titrant akışı durur.
Şekil-21: Otomatik, dönüm noktası ayarlı bir titratör
Şekil-21'de görülen titratörlerin
potansiyel değişikliğini algılamaları çok ani değildir ve dönüm noktasının
üzerine çıkma eğilimleri vardır. Bu sorunu yenmek için cihaza, hata sinyali
üzerine kare-dalga sinyali veren bir sistem yerleştirilir. Bu durumda selenoid
düğmesi sadece net sinyal, kare dalga sinyalini aştığı zaman kapanacak şekilde
ayarlanır. Sonra kare-dalga sinyallerinin frekansı tarafından kontrol edilen
miktarlarda titrant ilave edilir.
Kaydedici titratörler analitin
eğrisini çizerken titrasyona eşdeğerlik noktasından sonra da devam eder. Bazı
cihazlarda titrant ilavesi, bir milivolt kaydedicinin kağıt hızıyla uyumlu
olacak şekilde sabit bir hızda yapılır. Kalem yükseltilmiş hücre çıkış
potansiyelini zamanın fonksiyonu olarak çizer; burada zaman, titrant hacmiyle
orantılıdır.
Şekil-22: (a) Otomatik
kaydedici bir titratör, (b) teorik titrasyon eğrisi, (c) kaydedici tarafından
çizilen titrasyon eğrisi, (d) c ‘deki eğrinin açıklamalı genişletilmiş şekli
Kaydedici
titratörler, deneyimli bir kimyager gibi çalışırlar; dönüm noktası bölgesinden
önce ve sonra titrant ilavesini hızlı ve fazla miktarlarda yaparlar, dönüm
noktasına yaklaşıldığında ilave az miktarlarda ve yavaş yavaş yapılır. Şekil-23'de
böyle bir cihazın basitleştirilmiş şeması verilmiştir. Cihazın anahtar sistemi
yükseltilmiş hata sinyali sistemine göre çalışır; hata sinyali, elektrotların
potansiyelinin potansiyometrenin uyguladığı potansiyelden farklı olduğu zaman
çıkar. Bu potansiyometre, kaydedici kalemi ayarlayan bir motorun
kumandasındadır. Hata sinyali küçükse elektronik devre anahtarı şırınga tip
büretin motorunu ve kaydedicinin kağıt yürütücüsünü harekete geçirir; aynı
zamanda potansiyometre ve kalem yürütücü motor durdurulur. Hata sinyalinin
belli bir seviyenin üstüne çıkmasını sağlayacak yeterli miktarda titrant ilave
edildiğinde anahtarların açılıp-kapanma olayı tersine döner; bu halde büretten
titrant akışı ve kağıdın ilerlemesi dururken potansiyometre ve kalem
yürütücüler çalışır. Böylece Şekil-23c'de kaydedilmiş olan titrasyon eğrisinde
de görüldüğü gibi bir seri titrant ilavesi yapılır.
Tam
Otomatik Titratörler
Şekil-23: Tam otomatik bir titratör
Tam otomatik titratörlerde çok
sayıda örneğin konulabileceği dönen bir tabla bulunur. Bir örneğin titrasyonu
tamamlandıktan sonra çözelti otomatik olarak titrasyon sisteminden atılır, kap
ve elektrotlar çalkalanır, büret yeniden doldurulur, örnek tablası döner ve
sisteme ölçülen miktarda yeni bir örnek alınarak titre edilmeye başlanır. Böyle
bir sistem mikroprosessör ile kontrol edilir, hesaplamalar ve analitik
sonuçları kaydedici bilgisayar düzenekleri bulunur. Bunlar oldukça pahalı
cihazlardır, ancak çok sayıda rutin analizleri kısa zamanda yapabilmesi
nedeniyle parasını karşılayacak özelliklere sahiptirler.