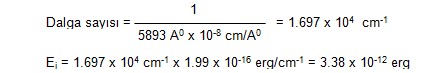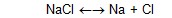Atomik spektroskopi, elektromagnetik ışının atomik
tanecikler tarafından absorbsiyonu (soğurulması), emisyonu (yayımlanması) ve
fluoresansı (tutulma ve çıkarılma) temeline dayanır. Atomik spektral veriler
spektrumun ultraviyole görünür ve X-ışınları bölgesinde elde edilir.
Ultraviyole ve görünür atomik spektranın elde edilebilmesi
için örneğin atomize edilmesi gerekir. Atomizasyonda moleküller parçalanır ve
gaz halinde elementer taneciklere dönüşür. Atomize edilmiş elementin emisyon,
absorbsiyon ve fluoresans spektrumu, element için karakteristik birkaç dalga
boyunda çıkan ayrı ayrı hatlardan oluşur. Titreşim ve dönme kuvantum halleri
bulunmadığından band spektrumları görülmez; bu nedenle geçiş olanağı sayısı
küçüktür. Atomik spektroskopiye dayanan çeşitli yöntemler Tablo-1'de
gösterilmiştir.
Tablo-1: Atomik Spektral Yöntemlerin Sınıflandırılması
ALEV
SPEKTROSKOPİSİNİN TEORİSİ
İnorganik tuzların sulu bir çözeltisi bir alevin sıcak
bölgesi içine püskürtüldüğünde metalik bileşenler indirgenerek elementel duruma
geçerler; aynı zamanda, az da olsa mono atomik iyonlar da meydana gelir.
Böylece alev içinde, elementer tanecikler içeren bir gaz çözeltisi veya
"plazma" oluşur. Alev spektroskopisi bu taneciklerin yaptığı
absorbsiyon, emisyon veya fluoresansı ölçer. Şekil-1'de üç tip alev spektroskopisi görülmektedir.
Şekil-1(a) "atomik emisyon" veya "alev
emisyonu" spektroskopisidir ve sıcak bir aleve püskürtülen örnek
çözeltisinden çıkan karakteristik hattın ışın gücünün ölçülmesi temeline
dayanır. Alevden ve örnekteki diğer bileşenlerden oluşan ışınları ölçülecek
ışından ayırmak için bir dalga boyu seçici (monokromatör veya filtre) kullanılır.
Bir "atomik
absorbsiyon" veya " alev absorbsiyon" cihazının şematik
görünümü Şekil-1(b)'de verilmiştir. Alev, herhangi bir fotometre veya
spektrofotometredeki hücre (veya küvet) görevini yapar; bu nedenle atomize
edilmiş örneğin seyreltik bir gaz çözeltisi gibi düşünülebilir. Uygun bir
kaynaktan gelen ışın atomize edilmiş örnekten geçer ve bir fotometre veya
spektrofotometrenin slitine girer. Kaynaktan gelen ışınla alevden çıkarılan
ışını ayırabilmek için, kaynak ışını aleve ulaşmadan önce bir chopperden
geçirilir. Dedektör devresi, alev emisyonundan oluşan doğru akım çıkışını
görmeyecek, fakat kaynaktan ve örnekten gelen alternatif akım sinyalini ölçecek
şekilde dizayn edilir.
"Atomik fluoresans" veya "alev
fluoresans" Şekil-1(c)'deki gibi şematize edilebilir. Burada da alev
örneği atomik taneciklere parçalar ve uygun bir kaynaktan gelen ışınla
uyarılmaları için bunları ışık yolu üzerinde tutar. Oluşan fluoresans bir fotometre
veya spektrofotometreye gönderilerek ölçülür.
Şekil-1: Üç tip alev spektrometresi
Alev Spektrası
Gaz halindeki atomik taneciklerin emisyon, absorbsiyon, ve
fluoresans spektraları, en dıştaki elektronların elektronik geçişleriyle doğan,
iyi-tanımlanan dar hatlar şeklindedir. Metaller için bu geçişlerin çoğu
ultraviyole ve görünür bölge enerji seviyelerinde olur.
Bir elementin dış elektronlarının enerji seviye
diyagramları, atomik spektroskopi cihazlarının temel çalışma ilkelerini oluşturur.
Şekil-2(a)'da görülen Na atomunun diyagramı tipik bir örnektir. Enerji skalası
elektronvolt (eV) birimine göre doğrusaldır; burada 3s orbitalinin enerji
değeri sıfırdır. Tek bir 3s elektronunu merkez atomun etkisinden kurtararak Na
iyonu elde edebilmek için gereken enerji 5.2 eV'dur ve bu değer Şekil-2(a)'daki
enerji skalasının üst sınırıdır.
Şekil-2: (a) Na atomu ve (b) Mg+
iyonunun, enerji seviye diyagramları
Şekil-3: Mg atomunun enerji seviye
diyagramı
Atomik orbitallerin enerjisi diyagramda yatay çizgilerle
gösterilmiştir. p orbitalleri, enerjileri birbirinden biraz farklı iki seviyeye
ayrılırlar. Bu farklılık şöyle açıklanabilir: Bir elektronun spinlerinin
hareket yönü kendi orbital hareketiyle aynı veya ters yönde olabilir.
Elektronun taşıdığı yük nedeniyle hem spin hem de orbital hareketleri magnetik
alanlar yaratır. İki hareketin yönlerinin ters olması durumunda doğan magnetik
alanlar birbirini çeker, tersine hareket yönlerinin aynı olması bir itme
kuvveti oluşturur. Sonuçta, spini kendi orbital hareketine zıt yönde hareket
eden elektronun enerjisi, aynı yönde hareket eden bir elektrona göre daha düşük
olur. d ve f orbitallerinde de benzer farklılıklar vardır, fakat fark sodyum
atomunda ölçülemeyecek kadar azdır; bu nedenle d orbitallerinde (Şekil-2a) tek
bir enerji seviyesi görülür.
Yüksek enerjili p, d ve f orbitallerinin iki hale ayrılması,
tek bir dış elektronu bulunan tüm atom veya iyonlarda görülür. Şekil-2(b)’deki
tek yüklü magnezyum iyonunun enerji seviye diyagramı bu nedenle yüksüz sodyum
atomunun diyagramına benzer. Dipozitif aluminyum iyonu ve diğer alkali metal
atomlarının diyagramları da Şekil-2'dekilere benzerler. Şu önemli hususu bilmek
gerekir: 3p ve 3s halleri arasındaki enerji farkı magnezyum iyonunda sodyum
atomuna göre yaklaşık iki kattır; bu durum magnezyum iyonundaki çekirdek
yükünün büyük olmasından kaynaklanır.
Şekil-2(b) ve 3'deki enerji diyagramları bir iyonun ve bu
iyona ait atomun değişik enerji seviye spektrumları verdiğini gösterir. Atomik
magnezyumun iki dış elektronu vardır ve farklı enerjilerde tekli (singlet) ve
üçüz (triplet) hallere uyarılırlar (Şekil-3). Tekli halde iki elektronun
spinleri ters yönlüdür (veya çiftleşmiş haldedir); üçüz halde spinler
paraleldir. Üçüz halin p, d ve f orbitalleri enerjileri birbirinden biraz
farklı üç seviyeye ayrılırlar. Bu durum iki dış elektronun spinleri ile tüm
elektronların orbital hareketlerinden doğan net alan arasındaki etki ile
açıklanır. Tekli halde iki spin çiftleşmiştir ve magnetik alanlar birbirini yok
ederler, böylece bir enerji ayrılması olmaz. Üçüz halde iki spinin momentleri
aynı yönde olduğundan çiftleşme şansı yoktur. Spinlerin toplam magnetik alanı
üzerindeki orbital magnetik momentin etkisiyle p seviyesi üçe bölünür. Bu
davranış tüm toprak alkali atomlar, tek yüklü Al ve Be iyonları, iki dış
elektronu bulunan diğer iyonlar, v.s., için karakteristiktirtir.
Dıştaki elektronların sayısı arttıkça enerji seviye
diyagramlarının karmaşıklığı da artar; üç dış elektron bulunduğunda enerji
seviyeleri ikiye bölünür ve dörtlü hal oluşur, dört elektron bulunduğunda ise
tekli, üçlü ve beşli haller oluşur.
Na ve Mg gibi elementlerin enerji seviye diyagramları ile
atomik spektraları arasındaki ilişki oldukça düzenlidir ve teorik tanımlamaya
uygundur; ancak ağır elementler ve özellikle geçiş metallerinde aynı uyum
görülmez. Bunlarda birbirine yakın çok sayıda enerji seviyesi bulunur; bunun
sonucu olarak da absorbsiyon veya emisyon hatlarının sayısı çoktur. Örneğin,
Harvey değişik elementlerin nötral ve tek iyonize atomlarının ark ve kıvılcım
spektralarında gözlenen hatların sayılarını incelemiştir. Alkali metallerde bu
sayı Li için 30'dan Cs için 645'e kadar değişen bir aralık gösterir; toprak
alkali metallerde Mg 173, Ca 662 ve Ba 472 hat verir. Geçiş metallerinden Cr
2277, Fe 4757 ve Ce için 5755 hattı bulunur. Alevde, sıcaklığın düşük olması
nedeniyle ayrılan hat sayısı daha azdır; yine de alev metallerinin geçiş
spektrası, atom numarası küçük olan elementlerin spektralarından çok daha
karmaşıktır.
Atomik Emisyon
Spektrası
Bir madde örneğinde bulunan tüm atomlar oda sıcaklığında
temel halde bulunurlar. Örneğin, metalik sodyumun tek dış elektronu bu
koşullarda 3s orbitalinde bulunur. Bu elektronun daha yüksek orbitallere
uyarılması için bir alevin ısısı veya bir elektrik arkı veya kıvılcım gerekir.
Uyarılmış atomun yaşam süresi çok kısadır, bir ışın kuvantumu çıkararak
(emisyon) temel haline geri döner. Şekil-2(a)'daki dik hatlar Na atomlarının
uyarılmasını takibeden bazı elektronik geçişleri gösterir. 5890 ve 5896 A0'deki
iki hat uyarılma koşullarında çok şiddetlidir ve analitik tayinlerde tanımlayıcı
hatlar olarak kullanılırlar. Slit genişliği, iki hattı anında ölçebilecek
şekilde ayarlanır.
Atomik Absorbsiyon
Spektrası
Bir alev plazmasındaki sodyum atomları, 3s halinden daha
yüksek uyarılmış hallere elektronik geçişlere olanak veren dalga boylarındaki
ışığı absorblayabilir. Örneğin, deneysel olarak 5890, 5896, 3302, ve 3303 A0‘de
keskin absorbsiyon pikleri elde edilmiştir; tekrar Şekil-2(a)'ya bakılırsa
birbirini takip eden her pik çifti (5890-5896 A0 ve 3302-3303 A0)
3s seviyesinden sırasıyla 3p ve 4p seviyelerine geçişleri gösterir. 3p den 5s
geçişiyle olan absorbsiyon çok zayıf olduğundan gözlenemez; çünkü bir alevdeki
3p halinde olan sodyum atomlarının sayısı çok azdır. Buna göre bir alevden elde
edilen atomik absorbsiyon spektrumu, temel halden en üst seviyelere geçişlerin
neden olduğu "resonans hatlarından" oluşur.
Atomik Fluoresans
Spektrası
Bir alevdeki atomlar ışın çıkararak fluoresans özellik
gösterebilirler; kaynak, elementin önceden absorbladığı dalga boylarındaki
ışındır. Moleküler fluoresansda olduğu gibi, fluoresans spektra ışık yoluna 900
lik açı altındaki bir yönde gözlenebilir. Gözlenen ışın resonans fluoresansın
bir sonucudur. Örneğin, magnezyum atomları bir ultraviyole kaynağa karşı
tutulduğunda 2852 A0 deki ışını absorblarlar ve elektronlar 3s den
3p seviyesine çıkarlar (Şekil-3). Atomların uyarılmış halde kalma süreleri çok
çok kısadır, aynı dalga boyundaki ışını emitleyerek tekrar 3s seviyesine
dönerler. Dönüşte resonans fluoresansı meydana gelir ve bu yöntemle yapılan
analizlerde kullanılan ışın da budur. Tersine bir durum sodyum atomlarının 3302
A0 dalga boyundaki ışını absorblamasında görülür; elektronlar 4p
haline geçerler (Şekil-2a). Buradan iki 3p haline ışımasız geçiş, resonans
fluoresansa kıyasla daha hızlı olur. Bu nedenle 3302 A0'de
fluoresans gözlenmez, sadece 5890 ve 5896 A0'de fluoresans oluşur.
Atomik fluoresans için üçüncü bir mekanizma tipi Şekil-4’de verilmiştir. Burada
bir alevde uyarılan bazı talyum atomlarının temel hale dönüşleri iki kademede
gerçekleşir; birincisi fluoresans kademesidir ve 5350 A0 ‘de bir hat
verir, bunu hemen ışımasız dönüş izleyerek atom temel hale ulaşır. Ayrıca 3776
A0'de resonans fluoresansı da gözlenir. Yani, talyum iki fluoresans
hattı verir.
Şekil-4: İki fluoresans hattı
gösteren talyumun enerji seviye diyagramı
Hat Genişlikleri
Atomik emisyon ve absorbsiyon pikleri, moleküllerin emisyon
ve absorbsiyon piklerine göre çok daha dardır. Gözlenebilen atomik hatların
tabii genişlikleri 10-4 A0 kadardır. Hatları
birleştirerek 0.02- 0.05 A0 genişliğe kadar artıran iki etkiden söz
edilebilir.
"Doppler genişlemesi", alev plazmasındaki atomik
taneciklerin hızlı hareketlerinden oluşur. Monokromatöre doğru hareket eden
atomlar Doppler-kayması nedeniyle düşük dalga boylarındaki ışınları emitlerler;
bu etki monokromatörden çıkan atomlarda tersine döner. Doppler genişlemesi
absorbsiyon hatlarında da gözlenir. Kaynağa doğru hareket eden atomlar, dik
yönde hareket edenlerin adsorbladığı ışından daha kısa dalga boylu ışın absorblarlar.
Kaynaktan zıt yöne gidenler için ise bunun tersi oluşur.
"Basınç genişlemesi" band genişliğini artıran
ikinci bir etkidir. Burada atomlar arasındaki çarpışma temel-hal enerji
seviyelerinde küçük değişikliklere neden olur ve bu da pikleri genişletir.
Alevlerde Moleküler
Spektra
Hidrojen veya hidrokarbon yakıtları bazı dalga boyu
aralıklarında absorbsiyon ve emisyon bandları verirler. Bandlar molekülün
alevde OH ve CN radikalleri ve C2 molekülleri içermesinden
dolayıdır. Bazı toprak-alkali ve nadir-toprak metalleri de uçucu oksit veya
hidroksitler oluşturarak geniş spektral bir bölgede absorbsiyon ve emisyon
yapabilirler. Şekil-5'de görülen CaOH'in absorbsiyon spektrası tipik bir
örnektir. Şekildeki noktalı hat baryum resonans hattı dalga boyudur. Baryumun
atomik absorbsiyon yöntemiyle tayininde daha sıcak alev kullanılarak ortamda
bulunan CaOH molekülünün parçalanması sağlanır; böylece şekilde görülen CaOH e
ait absorbsiyon bandı kaybolur. Band spektrum elementlerin yaklaşık üçte
birinin analizinde kullanılabilen bir analiz yöntemidir. Gerek emisyon gerekse
absorbsiyon spektroskopisinde spektrayı karıştıran istenmeyen bazı bandlar bulunur;
bunlar özel dalga boyu seçimi ve yakma koşullarının değiştirilmesi gibi önlemlerle
giderilmelidir.
Şekil-5: CaOH ve Ba için moleküler alev ve alev absorbsiyon spektraları
ALEV ÖZELLİKLERİ
Alev spektroskopisi yöntemlerinde uyumsuz sonuçlar elde
edilmesinin en önemli nedeni alevinin özelliklerindeki değişikliklerdir. Bu
nedenle alevlerin en önemli özelliklerinin ve bunları etkileyen değişkenlerin
bilinmesi zorunludur.
Alev Sıcaklığı
Tablo-2'de alev spektroskopisinde kullanılan bazı yakıtlar
ve oksitleyiciler ile bunların stökiyometrik oranlarda bulunduğu sıcaklıklar
verilmiştir.
Tabii gaz veya yakıt gazının havada yanmasıyla yüksek
sıcaklıklara ulaşılamaz, ancak çok düşük uyarılma enerjisi isteyen alkali ve
toprak-alkali metaller uyarılarak uygun spektralar verirler. Asetilen/hava
karışımları daha yüksek sıcaklık sağlar. Pek çok metalin uyarılması için
oksitleyici olarak oksijen veya azot monoksit kullanılmalıdır; normal
yakıtlarla sıcaklık 2500-3100 0C'ye kadar çıkarılabilir. En yüksek
alev sıcaklığına siyanojenin oksijen içinde yakılmasıyla ulaşılabilir.
Tablo-2: Çeşitli Yakıtlar ve Oksitleyiciler için En
Yüksek Alev Sıcaklıkları
Yüksek Alev Sıcaklıkları
Sıcaklık Profilleri
Şekil-6'da atomik spektroskopi için tipik bir alev sıcaklık
profili görülmektedir. En yüksek sıcaklık içteki koninin biraz üstünde bulunur.
Kalibrasyonda ve analitik ölçmelerde alevin bu kısmının giriş slitine
odaklanması, özellikle emisyon yöntemlerinde, çok önemlidir.
Şekil-6: Doğal gaz –hava alevinin
sıcaklık profili (0C olarak)
Spektra Tiplerine
Sıcaklığın Etkisi
Alev plazmasının sıcaklığı bir elementin gözlenen emisyon,
absorbsiyon, ve fluoresans spektrumunun yapısını belirler. Örneğin, Mg içeren
bir örnek düşük sıcaklıktaki (2000-2500 K) bir aleve püskürtüldüğünde element
tümüyle atomik hale geçer; spektrum Şekil-3'de görülen hatları içerir. Diğer
taraftan siyanojen alevi kullanıldığında elementin %50'den fazlası Mg+
iyonu şeklinde bulunur; bu durumda spektrumda Şekil-3'deki hatlar yanında
Şekil-2(b)'de verilen dalga boylarındaki hatlar da yer alır.
Emisyon, Absorbsiyon
ve Fluoresansa Sıcaklığın Etkisi
Alev sıcaklığı, uyarılmış halde bulunan atom veya
moleküllerin miktarını da etkiler; yani emisyonun şiddetini belirler; uyarılan
kısım Boltzmann denklemi ile hesaplanabilir. Uyarılmış ve temel haldeki
atomların sayıları sırasıyla Nj ve N0 ile gösterildiğinde
bunların oranı aşağıdaki denklemle verilir.
Burada k Boltzmann sabiti (1.38 x 10-16
erg/derece), T kelvin cinsinden sıcaklık, ve E j uyarılmış hal ile temel hal arasındaki erg
cinsinden enerji farkıdır. Pj ve P0 miktarları istatistik
faktörlerdir; bunlar her kuvantum seviyesindeki enerjileri eşit olan hallerin
sayıları ile belirlenir. Aşağıdaki örnekte görüldüğü gibi tipik bir gaz
alevindeki (T = 2500 K) uyarılmış atomların sayısı çok azdır.
ÖRNEK
Sodyum atomlarının 2500 ve 2510 K’de 3p uyarılmış haldeki
sayılarının temel haldeki sayılarına oranı nedir?
3p ® 3s geçişleri
yapan iki Na emisyon hattı vardır. Ortalama dalga boyu 5893 A0
alınarak Denklem(1)den Ej hesaplanır ve erg'e çevrilir.
3s seviyesinde iki, 3p seviyesinde altı kuvantum hali
vardır. Buna göre,
bulunur. Bu değerler Denklem(1)'de yerine konarak Nj
/ N0 oranı hesaplanır:
Bu örnek, alev sıcaklığında 10 K'lik bir değişikliğin,
uyarılmış Na atomları sayısını %4 kadar artırdığını gösterir. İki hattın
emitlediği ışının gücü de bununla paralel olarak artar. Örnekte de görüldüğü
gibi emisyon ölçümüne dayanan analitik analiz yöntemlerinde alev sıcaklığının
çok yakından kontrolü önemlidir.
Absorbsiyon ve fluoresans yöntemleri teorik olarak sıcaklığa
daha az bağımlıdır. Çünkü her ikisinde de ölçmelerde uyarılmamış atomların
sayısı önemlidir. Yukarıdaki örnekte, hidrojen/oksiyen alevinin sıcaklığında
sodyum atomlarının sadece %0.017'si termal olarak uyarılmış haldedir. Emisyon
yöntemi analitin bu küçük kısmı ile ölçme yapar. Absorbsiyon ve fluoresans
yöntemlerinde ise geri kalan %99.8'lik uyarılmamış Na atomlarının bulunduğu
kısım önemlidir. Alev sıcaklığının 100K atması halinde Na
iyonlarında %4'lük bir artış olur, oysa sodyum atomlarındaki değişiklik önemli
bir düzeyde değildir.
Sıcaklıktaki dalgalanmaların alev absorbsiyonu ve
fluoresansı ölçümlerinde dolaylı bazı etkileri vardır. Sıcaklıktaki artış
çoğunlukla atomizasyon işleminin verimini ve böylece alevdeki atomların
sayısını artırır. Ayrıca, atomik taneciklerin hareket hızı da artacağından
Doppler etkisi büyüyerek hatların genişlemesine, pik yüksekliğinin azalmasına
neden olur. Yüksek sıcaklıklarda gaz halindeki atomların konsantrasyonlarının
artmasıyla absorbsiyon hatları basınçla genişleme etkisine de uğrar. Bu dolaylı
etkiler nedeniyle kantitatif absorbsiyon ve fluoresans ölçümlerinde de alev
sıcaklığının kontrol altında tutulması önemlidir.
Alevlerdeki uyarılmamış/uyarılmış atomların oranının büyük
olması üç atomik alev yönteminde ilginç bir durum gösterir. Atomik absorbsiyon
ve fluoresans spektroskopide tanecik sayısı çoktur, bu nedenle ölçmelerin
emisyon işleminden daha hassas sonuç vereceği düşünülebilir. Oysa bir
absorbsiyon ölçümü (log P0 –log P) farkı olarak
değerlendirildiğinden tanecik sayısının çokluğu özellikle P0 ve P değerlerinin
birbirine yakın olması durumunda daha büyük hataya yol açar. Sonuç olarak,
atomik emisyon ve atomik absorbsiyon işlemleri uygulama yerine göre birbirleri
ile kıyaslanabilir hassasiyettedirler; bir grup element için biri daha hassas
iken bir başka grup elementte diğeri uygun hassasiyettedir.
Alev Profilleri
Bir alevdeki önemli bölgeler, alttan üste doğru taban, iç
koni, reaksiyon bölgesi, ve dış ceket (Şekil-7) şeklinde tanımlanır. Örnek
aleve küçük damlacıklar halinde tabandan girer. Bu bölgede örnekteki su
buharlaşır; bazı örnekler iç koniye katı tanecikler halinde girerler. İç konide
buharlaşma ve parçalanma ile atomik haller oluşur; uyarılma ve absorbsiyon
işlemlerinin olduğu yer de bu bölgedir. Reaksiyon bölgesinde atomlar oksitlerine
dönüşürler, dış ceket kısmına geçerler ve alevden dışarı atılırlar. Aleve
püskürtülen örneğin her damlacığı bu sırayı izlemez; taneciklerin büyüklüğü ve
püskürtülme hızına göre örneğin önemli bir kısmı alevden değişmemiş olarak
çıkar gider.
Bir alev profili alevin değişik kısımlarında oluşan işlemler
hakkında yararlı bilgiler verir; grafikten (Şekil-6) sıcaklık, kimyasal
bileşim, absorbans ve ışın veya fluoresans şiddeti gibi parametrelerle ilgili
ilginç bilgiler edinilebilir.
Şekil-7: Üç elementin alev
absorbsiyon profilleri
Emisyon Profilleri
Şekil-8'de görülen üç boyutlu profil bir siyanojen alevinde
elde edilen Ca hattının emisyon şiddetini gösterir. Burada emisyonun en
şiddetli olduğu yer alevin iç konisinin üzerinde bir noktadadır. Şekildeki
emisyon şiddetinin, örneğin aleve verilme hızına çok bağlı olduğu da
anlaşılmaktadır. Başlangıçta hattın şiddeti akış hızıyla (veya Ca
taneciklerinin sayısıyla) hızla yükselir, keskin bir maksimuma ulaşılır. Akış hızı
arttıkça örnekle beraber püskürtülen su da artacağından alevin sıcaklığı düşer
ve hattın şiddeti de azalmaya başlar.
Emisyon analizlerinde hat yerine moleküler band spektraları
oluşuyorsa, band pikleri çoğunlukla hat maksimumlarından daha önce çıkar.
Örneğin, kalsyum alevde CaOH halinde bulunduğundan (Şekil-5) 540-560 nm’de band
verir. Bu emisyon bandının şiddeti alevin iç koni bölgesinde maksimuma ulaşır
ve dış ceket bölgesinde hızla düşer; çünkü emisyonu yapan moleküller dış ceket
bölgesinin yüksek sıcaklığında
parçalanırlar.
Geliştirilmiş alev emisyon spektroskopi cihazlarında
monokromatörler bulunur, böylece alevin küçük bir kısmı ile çalışılır; alevin
giriş slitine göre konumu ayarlanır. Filtreli fotometrelerde ise alevin büyük
bir bölümü kullanılır; bunlarda alevin konumu fazla önemli değildir.
Şekil-8: Kalsiyum hattının alev
profili; farklı örnek akış hızları ve siyanojen-oksijen alevi kullanılmıştır
Absorbans Profilleri
Şekil-7'de üç elementin tipik absorbans profilleri
görülmektedir. Mg, iki zıt etki nedeniyle alevin ortalarında bir maksimum
verir. Taban kısımdan uzaklaştıkça alev ısısı ile karşılaşan element miktarı,
dolayısıyla atomik magnezyum miktarı arttığından absorbans da artar. Reaksiyon
bölgesinde Mg oksitlenmeye başlar. Oksitlenme, absorbansın azalmasına neden
olur; çünkü, oluşan oksit tanecikleri kullanılan dalga boyundaki ışını
absorblamazlar. Alev ayarlanıp maksimum absorbans elde edilerek en yüksek
analitik hassasiyete ulaşılabilir.
Gümüşde farklı bir absorbans profili görülür. Gümüş
oksitlenmeyen bir element olduğundan tabandan alevin en uç kısmına kadar
absorbansda artış görülür, çünkü alevdeki gümüş atomları sürekli olarak artar.
Bunun tam tersi bir durum kromda gözlenir. Cr kolay
oksitlenir ve oksitleri çok kararlıdır. Bu nedenle absorbans alevin tabanından
başlayarak sürekli olarak düşer; bu gözlem buradaki temel olayın oksit oluşumu
olduğunu gösterir. Alev absorbans profillerinden bu elementlerin her birinin
analizinde alevin farklı bölgelerinin kullanılması gerektiği açıkça
anlaşılmaktadır.
ATOMİK SPEKTROSKOPİ
ATOMİZERLERİ
Atomik spektroskopi cihazlarında iki tip atomizer bulunur.
Atomik emisyon, absorbsiyon, ve fluoresans ölçmelerinde kullanılan alev
atomizerleri ve sadece atomik absorbsiyon ile fluoresans ölçmelerinde
kullanılan alevsiz atomizerler.
Atomik Spektroskopi
Alev Atomizerleri
Atomik spektroskopide kullanılan en yaygın atomizasyon
sisteminde bir nebulizer ve bir yakıcı-bek (burner) kısım bulunur. Nebulizer
örnek ile gazın karışarak ince bir sprey veya aerosol şekline gelmesini sağlar.
Bekler türbülent (toplam harcamalı) ve laminar (ön karıştırmalı) akışlı
olabilir.
Türbülent Akışlı
Bekler
Şekil-9'da türbülent akışlı bir bek görülmektedir. Burada
nebulizer ve bek birleştirilmiş durumdadır. Örnek kapilere çekilir ve kapiler
ucu etrafındaki gaz akışının venturi etkisiyle gazla homejen bir aerosol yapar.
Örnek 1-3 ml/dak. hızla akar.
Türbülent akışlı bekler aleve çok miktarda ve örneği
tanımlayan bir akış sağlarlar, geri akış ve patlama ihtimali yoktur. Bu tip
beklerin dezavantajları arasında alev uzunluklarının az oluşu ve uç kısmın
tıkanma sorunları sayılabilir. Ayrıca hem elektronik devreler ve hem de
çıkardığı ses yönünden türbülent akışlı bekler oldukça gürültülüdür. Bazan emisyon
ve fluoresans analizlerde de bulunmasına rağmen bu bekler daha çok absorbsiyon
çalışmalarında kullanılmaktadır.
Şekil-9: Türbülent akışlı bir bek
Laminar Akışlı Bekler
Şekil-10'da tipik bir laminar akışlı bek diyagramı
görülmektedir. Örnek bir kapiler uçtan geçen oksitleyici ile aerosol haline
getirilir. Bu aerosol yakıtla karışır ve sonra ince tanecikleri geçiren fakat
diğerlerini ayıran bir seri bafıldan geçer. Bafılda ayrılan örneğin büyük kısmı
bir atık kabıyla bağlantılı karıştırma bölmesinde toplanır. Baffıldan geçen
aerosol, oksitleyici ve yakıt, 5-10 cm uzunluğunda alevi olan yarık şeklindeki
bir bekte yakılır.
Laminar akışlı beklerin alevi oldukça sessizdir ve uzunluğu
da fazladır. Bu özellikler deneyin hassas ve tekrarlanabilir olmasını sağlar.
Hatta tıkanma sorunu da yok denebilecek kadar azdır. Dezavantajlar ise, örnek
verilme hızının düşük oluşu (bu durum alev uzunluğu avantajı ile dengelenir) ve
karıştırma bölmesindeki karışımdan homogen olmayan buharlaşma ihtimaliyetidir
(böyle bir durumda analitik kararsızlık ortaya çıkar). Ayrıca karışımın
patlayıcı özellikte olması halinde herhangi bir geri akış tehlikeli durumlara
neden olabilir. Bunu engellemek için Şekil-10'daki beke basınç atma delikleri
konmuştur.
Şekil-10: Bir laminar akımlı bek
Yakıt ve Oksitleyici
Regülatörleri
Alev spektroskopisinde oksitleyici ve yakıt akışının en
uygun şekilde ayarlanması için ideal atomizasyon koşulları denemeyle
bulunmalıdır. Yakıt ve oksitleyici yaklaşık olarak stökiyometrik miktarlarda
karıştırılır.
Kararlı oksitler oluşturan metallerin analizinde indirgen
aleve gereksinim vardır; bu durumda yakıt miktarı stokiyometrik değerden daha
fazla olmalıdır. Akış hızları iğne vanalı ve çift diyaframlı basınç
regülatörleri ile yapılır.
Aynı (tekrarlanabilir) analitik koşulların sağlanabilmesi
için yakıt ve oksitleyici sistemlere uygun flowmetreler takılır. En çok
kullanılan flowmetre rotametre tipinde olanıdır. Rotametre dar kısmı aşağıya
gelecek şekilde dikey olarak yerleştirilen çok az konik şeffaf bir tüptür.
İçinde konik veya küresel hafif bir malzeme bulunur. Gaz akışı bu malzemeyi
(dikey tüpteki yüksekliği gaz akış hızını gösterir) yukarı kaldırarak
kenarlarındaki boşluklardan geçer.
Alevsiz Atomizerler
Standard limitler içinde birbirine yakın sonuçlar
alınabilirlik yönünden alev atomizasyonu en üstün yöntemdir. Örnek verimi (ve
tabii hassasiyet) yönünden ise diğer atomizasyon yöntemleri tercih edilir.
Alevde örnek verimini düşüren iki neden vardır. Birincisi, alınan örneğin büyük
bir kısmı geri döner (laminar bek) veya tümü atomize adilemez (türbülent bek).
İkincisi, her atomun optik yoldaki alıkonma zamanı çok kısadır (10-4
s).
1970'li yıllarda alevsiz atomizerler kullanılmaya başlandı.
Bu sistemlerde örneğin tümü atomize edebilmektedir ve atomların optik yoldaki
ortalama alıkonma süreleri bir sn. veya daha fazla olduğundan hasassiyetleri
yüksektir.
Alevsiz bir atomizerde bir kaç mikrolitre örnekle çalışılır.
Örnek elektrikle ısıtılan karbon, tantal veya iletici başka bir metal üzerinde
düşük sıcaklıkta buharlaştırılır ve kül edilir. İletici özel (hallow) bir tüp,
bir şerit veya çubuk, bir kayıkcık veya bir çukurluktur. Örnek kül olduktan
sonra akım 100 A veya daha fazlaya çıkarılarak sıcaklık 2000-3000 0C
ye yükseltilir, bir kaç dakika içinde atomizasyon olur. Isıtılan ileticinin
hemen üstündeki bir bölgede atomize taneciklerin absorbsiyon veya fluoresansı
ölçülür. Absorbsiyon veya fluoresansın olduğu bir dalga boyunda algılanan
sinyal birkaç saniyede maksimuma yükselir ve sonra sıfıra düşer; bu gözlem
atomizasyonun hemen arkasından buharlaştırılmış örneğin ortamdan uzaklaştığını
gösterir. Analizler pik yüksekliği veya pik alanına göre yapılır. Atomizasyonda
ileticinin oksitlenmesine engel olmak için bir inert gaz ortamında çalışılır.
Alevsiz atomizerlerle çok az miktarlardaki örneklerle çok
hassas sonuçlar alınır. Örnek miktarı 0.5-10 mikrolitre civarındadır; bu mutlak
limitlerin 10-10–10-13 g analit aralığında olması
demektir. Böyle bir hasassiyet alevde ulaşılan hassasiyetin 1000 katıdır.
Alevsiz yöntemin relatif hassasiyeti %5-10 aralığındadır, alev atomizasyonunda
bu oran %1-2 dir.
Atomik absorbsiyon spektroskopisi diğer iki atomik
spektroskopik yöntemlerden daha çok kullanılır, çünkü cihaz rutin analizlerde
fazla tecrübeli olmayan teknisyenlerin bile kolaylıkla çalışabileceği şekilde
dizayn edilmiştir.
Atomik Absorbsiyon Yöntemlerinde
Kaynaklar
Atomik absorbsiyona dayanan analitik yöntemler, absorbsiyon
hatlarının çok dar ve elektronik geçiş enerjilerinin her element için farklı
olması nedenlerinden seçiciliği çok yüksek yöntemlerdir. Diğer taraftan, hat
genişliklerinin çok az olması moleküler absorbsiyonda karşılaşılmayan ölçme
sorunları yaratır. Beer kanunu sadece monokromatör ışına uygulanabilir
(absorbsiyon ile konsantrasyon arasındaki doğrusal ilişkiyi verir) ve kaynağın
band genişliğinin absorbsiyon pikinin genişliğine göre daha az olmasını
gerektirir. Bir atomik absorbsiyon hattının genişliği (0.002- 0.005 nm) kadar
ışın bandı verebilecek bir monokromatör yoktur. Bu durumda sürekli bir kaynak
kullanıldığında monokromatörden bir dalga boyunda gelen ışının çok az bir bölümü
absorblanır; çıkan bandın şiddeti, gerçekte o bandı oluşturan ışının şiddetine
göre küçüktür. Bu koşullarda Beer kanunu uygulanamaz ve yöntemin hassasiyeti de
önemli derecede düşer.
Bu sorun, absorbsiyon analizinde kullanılan dalga boyu (bir
tane) ile aynı dalga boyunda bir hat emitleyen ışın kaynağı kullanılarak
çözülebilir. Örneğin, sodyumun absorbsiyon analizinde 589.6 nm'deki hat ile
çalışıldığında kaynak olarak bir Na buharı lambası kullanılır. Gaz Na atomları
lamba içinde elektrik boşalması ile uyarılırlar; uyarılan atomlar düşük enerji
seviyelerine dönerlerken ışın çıkarırlar (emisyon). Çıkan ışın resonans
absorbsiyon hattı ile aynı dalga boyundadır. Özel olarak dizayn edilen bir
kaynak ile band genişlikleri absorbsiyon band genişliklerinden daha dar olan
emisyon hatları elde edilebilir. Örneğin, kaynak alev sıcaklığından daha düşük
bir sıcaklıkta çalıştırılarak Doppler genişleme etkisi çok azaltılır.
Absorbsiyon ölçmelerinde çıkan emisyon bandını yok eden bir monokromatörle
sadece absorbsiyon spektrumu elde edilebilir (Şekil-11).
Böylece, analizde kullanılan ışın, absorbsiyon pikinin band
genişliğini ölçebilecek şekilde sınırlandırılmış olur. Bu koşullarda Beer
kanununa uygunluk ve hassasiyet daha yüksektir.
Her element (veya element grubu) için ayrı bir lamba
kaynağına gereksinim vardır. Bu sıkıntılı durum, sürekli bir kaynak ve ayırma
gücü çok yüksek olan bir monokromatör kullanılarak karşılanabilir; yüksek
sıcaklıktaki alev içine elementin bir bileşiği verilerek bir hat kaynağı elde
edilir. Ancak bu tip önlemler her elemente özel lamba kullanılması kadar tatmin
edici olmaz.
Şekil-11: Atomların rezonans hatları
tarafından yapılan absorbsiyon
Hallow Katot (Oyuk
Katot) Lambalar
Atomik absorbsiyon ölçmelerinde kullanılan en uygun kaynak
Hallow katot lambalarıdır. Bunlarda kapalı bir cam tüp içinde tungsten bir anot
ile silindirik bir katot bulunur. Cam tüp 1-5 torr basınçta neon veya argon ile
doldurulmuştur (Şekil-12), katot, spektrumu alınacak metalden yapılmıştır.
Elektrodlar arasına bir potansiyel uygulandığında gaz
iyonlaşır ve iyonların elektrodlara doğru hareket etmesiyle 5-10 mA dolaylarında bir akım doğar. Eğer potansiyel
yeteri kadar büyükse gaz halindeki katyonların kinetik enerjisi katot yüzeyinden
bazı metal atomlarını çıkarabilecek ve bir atomik bulut yaratabilecek seviyededir;
bu işleme "püskürtme" denir. Püskürtülen metal atomlarının bir kısmı
uyarılmış haldedirler ve bilinen şekilde kendi karakteristik ışınını yayarlar.
Sonunda metal atomları katot yüzeyine veya tüpün cam duvarlarına geri
düfüzlenir. Katodun silindirik yapısı ışını tüpün belirli bir bölgesinde
yoğunlaştırır; bu dizayn geri dönen metal atomlarının cam duvarlar yerine
katoda yönelmelerini de sağlar.
Hallow katot lambanın verimi geometrisine ve çalışma
potansiyeline bağlıdır. Yüksek potansiyeller, dolayısıyla yüksek akımlar daha
büyük şiddette ışın yaratırlar. Bu avantaj, emisyon hatlarında Doppler
genişlemesi etkisinin artışı nedeniyle kısmen azalır. Ayrıca, yüksek akımlar
atom bulutundaki uyarılmamış atomların sayısını da artırır; bunlar ise
uyarılmış atomlardan çıkan ışını absorblama yeteneğindedirler. Bu
kendini-absorblama, özellikle emisyon bandının merkezinde, ışının şiddetini
düşürür.
Hallow katot tüpleri çeşitli şekillerde üretilir.
Bazılarının katotları bir kaç metal karışımından hazırlanır; bu tip lambalarla
bir elementten daha fazla elementin analizi yapılabilir.
Gaz Boşalım(Deşarj)
Lambaları
Gaz boşalım lambaları, metal atomları buharından elektrik
akımı geçirilmesiyle bir hat spektrumu verirler; örnek olarak Na ve Hg
lambaları gösterilebilir. Bu tip kaynaklar özellikle alkali metallerin
spektralarını elde etmekte kullanılır.
Kaynak Düzenlemesi
(Modülasyon)
Tipik bir atomik absorbsiyon cihazında, alevden çıkan ışının
neden olduğu girişimler giderilmelidir. Çıkan ışının çoğu alev ve dedektör
arasına yerleştirilen monokromatör ile uzaklaştırılabilir; yine de böyle bir
sistemle analizde kullanılacak seçilmiş bir dalga boyundaki alev ışını ortamdan
uzaklaştırılamaz. Alev, analitteki bazı atomların neden olduğu uyarma ve ışın
emisyonu sonucunda hala bulunmaması gereken (analizde kullanılan dalga
boylarındaki) ışınları içerir. Bu sıkıntılı durum kaynak çıkışı düzenlenerek
giderilebilir; kaynaktan gelen ışının şiddeti sabit bir frekansta dalgalanacak
şekilde ayarlanır. Bu durumda dedektör iki tip sinyal alır, kaynaktan gelen
değişken sinyal ve alevden gelen sürekli sinyal. Bu sinyaller uygun tipte
elektrik akımına dönüştürülür. Basit bir yüksek-geçişli RC filtre ile
düzenlenmemiş DC sinyalleri uzaklaştırılırken AC sinyalleri geçirilerek
yükselticiye gönderilir.
Kaynaktan gelen ışını basit ve etkili bir şekilde düzenleme,
kaynak ve alev arasındaki ışın demetine dairesel bir disk konularak yapılır.
Diskin her dörtte birlik dilimi, ışığı geçirecek şekilde sıra ile çıkarılır.
Disk sabit bir hızla döner ve istenilen frekansta ışının geçmesini sağlar.
Başka bir düzenleme yönteminde ise kaynağın gücü alternatif akım veya kesikli
akım kullanılacak şekilde dizayn edilebilir.
Atomik Absorbsiyon
Spektroskopisi Cihazları
Atomik absorbsiyon çalışmalarında kullanılan çeşitli
firmaların ürettiği cihazlar vardır. Cihazlar basit veya karmaşık olabilir ve
fiatları da değişiktir; tabii kullanım yeri ve amacına göre seçim yapılmalıdır.
Tek - Işın Yollu
Spektrofotometreler
Çok sayıda elementin analizinde kullanılan tipik bir
tek-ışın yollu cihazda bir kaç tane hallow-katot kaynağı, bir chopper, bir
atomizer ve fotomultiplier dedektörlü basit bir spekrofotometre bulunur. Cihaz,
moleküler absorbsiyon çalışmalarında kullanılan tek-ışın yollu cihaz gibi
çalışır. karanlık (dark current) transduserin önündeki bir kapak ile
sıfırlanır. Sonra aleve püskürtülen (veya alevsiz bir atomizerde yakılan) bir
şahit ile %100 T ayarı yapılır; sora şahit yerine örnek konularak geçirgenliği
saptanır.
Tek-ışın yollu atomik absorbsiyon cihazları daha önce
incelenen moleküler absorbsiyon cihazları ile benzer avantaj ve dezavantajlar
gösterir.
Çift - Işın Yollu
Spektrofotometreler
Şekil-13'de bir çift-ışın yollu cihazın şematik diagramı
görülmektedir. Hallow katot kaynaktan gelen ışın aynalı bir chopperde ikiye
ayrılır ve yarısı alevden geçerken diğer yarısı alevin etrafından dolaşır. İki
ışın daha sonra yarım-gümüşlenmiş bir aynada tekrar birleştirilerek bir
Czerney-Turner gratingli monokromatöre gönderilir; bir fotomultiplier tüp
transduser görevi yapar. Fotomultiplier çıkışı, chopperi döndüren sistemle
bağlantılı olarak çalışan amplifiere girer. Referans ve örnek sinyallerinin
oranı burada yükseltilir ve okuyucuya gönderilir; okuyucu ibreli bir metre veya
bir kaydedici olabilir. Başka bir dizaynda referanstan gelen ve yükseltilen
sinyal bir potansiyometre ile örnek sinyali ile kıyaslanabilecek bir düzeye
indirilir ve hareketli telin bulunduğu yerden, geçirgenlik veya absorbans
okunur.
Atomik absorbsiyon cihazlarında referans ışının alevden
geçmediğini ve bu nedenle de alevin yarattığı absorbsiyon veya saçılmadan
kaynaklanan ışın gücü kaybı olmadığını belirtmek gerekir.
Şekil-13: Tipik bir çift demetli
atomik absorbsiyon spektrofotometresi
Atomik Absorbsiyon
Spektroskopisi Uygulamaları
Atomik absorbsiyon spektroskopisi 60'dan fazla elementin
hassas tayininde kullanılabilen bir cihazdır. Örnek hazırlama ve her elementin
kantitatif analizi ile ilgili detaylar bu konudaki çeşitli kitaplardan
bulunabilir.
Hassasiyet ve Tayin
Sınırları
Atomik absorbsiyon yöntemlerini tanımlarken iki terim
kullanılır. Bunlardan biri "duyarlıkt"tır ve bir elementin 0.99
geçirgenlik sinyali veya buna eşdeğer 0.0044 absorbans sinyali verebildiği
konsantrasyon (mg/ml) olarak tarif
edilir. Modern atomik cihazlar 0.0044 den daha küçük absorbans sinyallerini
algılayabilecek hassasiyettedirler. Bu nedenle ikinci terim olan "tayin
(belirtme) sınırları" tanımı önem kazanır. Tayin sınırları, bir elementin,
cihaz sinyali standard sapmasının iki katına eşit analitik bir sinyal
verebildiği konsantrasyonu şeklinde tarif edilir (Alev atomizasyonu için cihaz
sinyali standard sapması, aleve şahit (kör) verildiği zaman elde edilen sinyal
değişikliklerinden elde edilir). Alev sıcaklığı, spektral band genişliği,
dedektör hassasiyeti, ve sinyal verme sistemi gibi değişkenler duyarlık ve
tayin sınırlarının önemli derecelerde değişmesine neden olurlar.
Atomik absorbsiyonda alev atomizasyonu yöntemi
uygulandığında çeşitli metalik elementler için tayin sınırları 3x10-4 ppm'den 20 ppm'e kadar değişir. Alevsiz
atomizasyonda bu sınırlar 10 katından 1000 katına kadar genişleyebilir.
Tablo-3'deki üç ve dördüncü kolonlarda alevli ve alevsiz
atomizasyon işlemlerinde bazı elementlerin tayin sınırları verilmiştir.
Normal çalışma koşullarında alev absorbsiyonu çalışmalarının
relatif hatası %1-2 dolaylarındadır. Özel dikkat ve önlemlerle bu sınır binde
birkaç seviyelerine indirilebilir.
Spektral Girişimler
(Engellemeler)
Atomik absorbsiyon yöntemlerinde iki tür girişimle
karşılaşılır. Birincisi, girişim yapıcı maddelerin absorbsiyonunun, analitin
absorbsiyonunun çok yakınına veya üstüne düşmesidir; monokromatörün ayırma gücü
bunları birbirinden ayırmaya yetmez ve "spektral girişimler" olur.
Diğeri "kimyasal girişimler" dir; burada, atomizasyon sırasında
oluşan çeşitli kimyasal işlemler analitin absorbsiyon özelliklerini bozar.
Spektral girişimlere aşağıda kısaca değinilecektir; kimyasal girişimlerin nedenleri
ise bir sonraki kısımda görülecektir.
Tablo-3: Bazı Elementlerin Atomik Absorbsiyon ve Alev Emisyon Spektrometre
ile Analizlerinde Tayin Sınırları


Hallow katot kaynaklarının emisyon hatlarının çok dar olması
nedeniyle atomik spektral hatların üst üste gelme olanağı çok azdır. Böyle bir
girişimin olması için iki hat arasında 0.1 A0'den daha az bir aralık
bulunmalıdır. Örneğin, aluminyum analizinin yapıldığı 3082.15 A0'lük
band, ortamda vanadyum bulunması halinde vanadyumun 3082.11 A0'lük
bandı tarafından engellenir. Böyle bir durumda aliminyumun 3092.7 A0
deki bandı kullanılarak girişimden kurtulunur.
Geniş band absorbsiyonu veya ışın saçan tanecikler veren
yanma ürünleri de spektral girişimlere neden olurlar. Her iki halde de geçen
ışının gücü azalır ve pozitif analitik hatalar doğar. Bu ürünlerin kaynakları
sadece yakıt ve oksitleyici karışımı ise, aleve bir şahit püskürtülerek
absorbsiyonu ölçülür ve elde edilen değerle gerekli düzeltmeler yapılır. Bu tip
düzeltme tek-demetli spektrometrelerde gerekli olduğu gibi çift-demetlilerde de
yapılmalıdır; çünkü çift-demetli cihazlarda referans ışın alevden geçmez
(Şekil-13).
İstenmeyen absorbsiyona veya saçılmaya neden olan taneciklerin
örneğin matriksinde bulunması halinde karşılaşılan sorun daha da önemlidir.
Böyle bir durumda geçen ışının P gücü örnek matriksindeki analite ait olmayan
maddeler tarafından azaltılırken gelen ışının P0 gücü aynı kalır;
sonuçta absorbansda dolayısıyle konsantrasyonda positif bir hata doğar. Böyle
bir potansiyel matriks engellemesine (absorbsiyon ile) örnek olarak toprak
alkali metaller karışımında baryum tayini gösterilebilir. Şekil-5'de görüldüğü
gibi atomik absorbsiyonda kullanılan baryum hattının dalga boyu (noktalı hat)
CaOH'in absorbsiyon bandının merkezinde bulunur; bu durum baryum analizinin
kalsiyum yanında engelleneceğini açıkça göstermektedir. Bu özel durumda
asetilen ve oksitleyici olarak azot oksit (hava yerine) kullanılır; yüksek
sıcaklık CaOH'i parçalar ve absorbsiyon bandının oluşmasını engeller.
Atomizasyon ürünlerinin neden olduğu saçılmadan kaynaklanan
spektral engelleme Ti, Zr ve W gibi elementleri içeren derişik (konsantre)
çözeltilerin aleve püskürtülmesinde oluşur; bu elementler alevde çok kararlı
metal oksitlerine dönüşürler. Tanecik çapları ışığın dalga boyundan daha büyük
olan metal oksitleri gelen ışığın önemli bir kısmının saçılarak uzaklaşmasına
sebep olurlar.
Bu gibi (matriksde bulunma) spektral girişimlerle çok sık
karşılaşılmaz ve karşılaşıldığı zaman da çoğu kez sıcaklık, yakıt/oksitleyici
oranı gibi analitik parametreler değiştirilerek girişimden kaçınılabilir. Başka
bir yöntem de, girişim kaynağının bilinmesi halinde örnek ve standardlara
girişim maddesinin fazlasının ilavesidir; bu durumda örnek matriksindeki
önleyici miktarı önemsiz bir seviyeye düşeceğinden etkisi de önemli olamaz.
İlave edilen maddeye "ışın tamponu" denir.
Kompleks örneklerde girişim kaynağı bilinmeyebilir; bunlarda
taban düzeltme yöntemi uygulanmalıdır. Çok kullanılan bazı düzeltme yöntemleri
aşağıda verilmiştir.
İki - Hat Düzeltme
Yöntemi
İki hat düzeltme işleminde bir kaynak referans hattına
gereksinim vardır; bu hat analit hattına çok çok yakın bir dalga boyunda
bulunmalı, fakat analit tarafından absorblanmamalıdır. Bu koşullarda, referans
hat gücündeki herhangi bir azalmanın (kalibrasyon sırasında gözlenir), örneğin
matriks ürünlerinin yaptığı absorbsiyon veya saçılmadan olduğu kabul edilir; bu
azalma, analit gücünü düzeltmede kullanılır.
Referans hat hallow katot lambasındaki bir safsızlıktan elde
edilebilir. Lambada bulunan gazdan bir neon veya argon hattı alınabilir veya
tayin edilecek elementin zayıf bir emisyon hattı kullanılabilir.
Sürekli - Kaynak
Düzeltme Yöntemi
Zemin (taban) düzeltmesinde kullanılan ikinci bir yöntem
çift-demetli cihazlara uygulanabilen sürekli-kaynak düzeltme yöntemidir. Burada
sürekli ışın kaynağı olarak bir H veya D lambası kullanılır (UV bölge).
Chopperin Şekil-13'deki konumu değiştirilerek, sürekli kaynaktan ve hallow
katot lambadan gelen ışını sıra ile alevden geçirecek şekilde ayarlanır. İki
kaynaktan gelen ışınların gücü, hallow katot kaynağından gelen bir örnek ve
referansın gücü ile kıyaslanır. Slit açıklığı, örnek atomlarının sürekli
kaynakdan absorbladığı kısım önemsiz olacak derecede geniş tutulur. Bu durumda
sürekli kaynağın alevden geçerken gücündeki azalma, sadece alevdeki maddelerin
neden olduğu saçılmayı veya geniş band absorbsiyonunu yansıtır.
Zeeman Etkisi
Düzeltme Yöntemi
Zemin düzeltmesinin Zeeman etkisinden yararlanılarak
yapıldığı ticari atomik absorbsiyon cihazları da vardır. Zeeman etkisinde
analit hattı, dalga boyları birbirinden 0.01 nm gibi çok az farklı iki kısma
ayrılır. Bu iki kısım birbirine göre 900 de polarize olmuşlardır ve
ışın yolu içine konan bir döner polarizer ile sıra ile izlenebilirler. Burada
atılan kısım absorbsiyon pikinden yeterli derecede ayrılabilir ve zemin
absorbsiyonu veya saçılması düzeltmesinde kullanılır.
Zeeman yarılması, atomizer veya ışık kaynağının kuvvetli bir
magnetik alana gönderilmesiyle sağlanır.
Kimyasal Girişimler
(Engellemeler)
Kimyasal girişimlerle spektral girişimlere göre daha çok
karşılaşılır. Uygun koşulların seçilmesiyle bu gibi etkiler en düşük düzeye
indirilebilirler.
Teorik ve deneysel veriler, bir alevin dış ceket kısmında
oluşan reaksiyonların denge konumuna yakın olduğunu gösterir. Bu durumda alevin
yanan gazları, termodinamik hesapların uygulanabileceği bir çözgen ortamı gibi
kabul edilebilir. Buradaki temel kimyasal reaksiyonlar arasında uçuculukları
düşük maddelerin oluşması, disosiyasyon, ve iyonizasyon reaksiyonları
sayılabilir.
Uçuculukları Düşük
Maddelerin Oluşması
En önemli girişim analit ile uçuculuğu az olan bileşikler
oluşturan anyonların neden olduğu girişimdir; bu tür bileşikler atomizasyon
hızını azaltırlar. Sonuçta düşük değerler elde edilir. Örneğin, sülfat veya
fosfat anyonlarının bulunduğu bir ortamda kalsyum absorbansı azalır. Kalsyum
konsantrasyonu sabit tutulduğunda, artan sülfat veya fosfat iyonları ile
absorbans değeri doğrusal olarak azalır ve azalma anyon/kalsyum oranı 0.5
oluncaya kadar sürer; bu orana ulaşıldığında absorbans gerçek değerinin
%30-50'sine kadar düşer ve bundan sonra anyon konsantrasyonundan etkilenmez.
Katyon girişimi de önemli bir konudur. Örneğin magnezyum
tayinin yapıldığı bir ortamda aliminyumun bulunması gerçek değerinden daha
düşük sonuçlar alınmasına yol açar; Böyle bir durumda ısıya dayanıklı
aluminyum-magnezyum bileşiği (belki bir oksid) oluşur.
Uçuculuğu düşük bileşiklerin sebeb olduğu girişimler daha
yüksek sıcaklıkta alevler kullanılarak giderilebilir. Ayrıca, "çıkarma
maddeleri" denilen bazı katyonlar kullanılarak girişimci anyonların analit
ile reaksiyona girmesi önlenebilir; anyonlar analit yerine bu tür katyonlarla
reaksiyona girerler. Örneğin, stronsyum veya lantanyum iyonunun fazlasının
ilavesiyle kalsiyum tayininde fosfat anyonlarının girişim etkisi en düşük
seviyeye indirilebilir. Bu iki katyon aluminyumun bulunduğu bir ortamda
magnezyum tayininde çıkarma maddeleri olarak kullanılır. Her iki durumda da
stronsyum veya lantanyum, girişimciler ile bileşik yapan analiti bileşikten
çıkararak onun yerine geçerler.
Analit ile uçucu fakat kararlı maddeler oluşturarak girişim
etkileri önleyen bazı "koruyucu maddeler" vardır. Bu amaçla çok
kullanılan üç koruyucu madde EDTA (etilen diamin tetra-asetik asit),
8-hidroksikinolin ve APDC(1-pirolidin-karboditioik asit amonyum tuzu) dir.
EDTA, kalsyum tayininde aluminyum, silikon, fosfat ve sülfat girişimini önler.
Kalsyum ve magnezyum tayinlerinde aluminyumun yaptığı girişim de
8-hidroksikinolin ile giderilir.
Disosiyasyon Dengesi
Bir alevin sıcak gaz ortamında sayısız disosiyasyon
(ayrışma) ve asosiyasyon (birleşme) reaksiyonları oluşarak metalik bileşikler
elementel hale geçerler. Bu reaksiyonların bazıları geri dönüşümlüdür ve
termodinamik kanunlar uygulanabilir. Bu nedenle teorik olarak denge aşağıdaki
şekilde tanımlanabilir.
Bir alevdeki kimyasal reaksiyonların yapısı hakkında sulu
çözeltilerde olduğu gibi yeterli kantitatif bilgiler yoktur. Ancak deneysel
gözlemlere göre hareket edilir.
Metal oksitler ve hidroksidlerin disosiyasyon reaksiyonları
bir elementin emisyon veya absorbsiyon spektrasının yapısını tayinde önemlidir.
Örneğin, disosiyasyon enerjileri 5 eV dan fazla olan toprak-alkali metal
oksidleri veya hidroksitlerin bulunması nedeniyle oluşan moleküler bandlar bu
metallerin spektralarının kuvvetli olmalarını sağlar. Çok yüksek sıcaklıklar
dışında, bu bandlar ayni metallerin atomları veya iyonlarının verdiği hatlardan
daha şiddetlidir. Tersine bir durum alkali metallerin oksitlerinde görülür; bu
oksitler çok fazla disosiye olduklarından, çok düşük sıcaklıklarda bile bu
elementlerin atom veya iyonlarının hat spektrumları moleküler (oksitler) band
spektrumlarından daha yüksektir.
Anyonların (oksijen hariç) disosiyasyon dengeleri alev
emisyonunu da etkiler. Örneğin, sodyumun hat spektrumu, ortamda HCl
bulunduğunda önemli derecede azalır. Bunun açıklaması denge üzerindeki
kütle-hareketi etkisiyle yapılabilir.
İlave edilen HCl klor atomlarını artırır ve bu durumda ortamdaki atomik sodyumun konsantrasyonu azalır; sonuçta hattın spektrumu düşer.
Bu tür girişime başka bir örnek aluminyumun ve titanyumun
bulunduğu halde vanadyum absorbsiyon hattının şiddetinin artmasıdır. Yakıtça
zengin alevlerde girişim daha şiddetlidir. Bu durum üç metalin, alevlerde
bulunan O ve OH ile etkileşmesiyle açıklanabilir. Oksijenli maddeler Ox genel
formulü ile gösterildiğinde bir seri denge reaksiyonu yazılabilir.
Yakıtça zengin yanma karışımlarında Ox konsantrasyonu
oldukça büyüktür ve örnekte aluminyum veya titanyum bulunduğunda konsantrasyon
daha da azalır. Ox konsantrasyonundaki azalma birinci denklemin sağ tarafa
kaymasına, metal konsantrasyonunun ve absorbansın artmasına neden olur. Yakıtça
fakir yanma karışımlarında ise Ox konsantrasyonu metal atomlarının toplam
konsantrasyonuna göre oldukça yüksektir. Aluminyum veya titanyum ilave
edildiğinde Ox'de az bir değişiklik olur ve birinci denklemin durumunda önemli bir
bozulma olmaz.
Alevlerde İyonizasyon
Atom ve moleküllerin yanma karışımlarındaki iyonizasyonu
azdır, ve oksitleyici olarak hava kullanıldığında ise ihmal edilebilir
düzeydedir. Yüksek sıcaklıktaki oksijen ve azot oksit alevindeki iyonizasyon
önemlidir, aşağıdaki denkleme göre oluşan serbest elektron konsantrasyonu oldukça yüksektir.
M nötral bir atomu veya molekülü, M+ iyonunu
gösterir. Burada M, metal atomudur.
Reaksiyonun K denge sabiti,
eşitliği ile verilir. [ ] terimleri içindeki ifadeler
aktiviteler, x, M'nin iyonize olan kısmı, ve p iyonizasyondan önce gaz
solventte bulunan metalin kısmi basıncıdır. Sıcaklığın K üzerindeki etkisi
"Saha denklemi" ile verilir.
Burada Ei metalin elektron volt olarak
iyonizasyon potansiyeli , T ortamın mutlak sıcaklığı, ve g her bir maddenin
statistik ağırlığıdır (maddeler g'nin altında belirtilmiştir). Denklemdeki son
terim alkali metaller için sıfır, toprak alkali metaller için de 0.6 dır.
Tablo-4'de, alev emisyon spektroskopide uygulanan koşullarda bazı metallerin
iyonizasyon dereceleri (hesaplanmış) verilmiştir. Sıcaklıklar, sırasıyla
hava/yakıt, oksijen/ asetilen, ve oksijen/siyanojen alevlerine aittir.
İyonizasyon işleminin bir denge reaksiyonu olması
(ürünlerden biri serbest elektronlardır) bir metalin iyonizasyon derecesinin
alevdeki diğer iyonlaşabilen metallerin bulunmasından etkilendiğini gösterir.
Buna göre ortamda sadece M elementi değil de B elementi de varsa ve B aşağıdaki
eşitliğe göre iyonlaşıyorsa,
M nin iyonizasyon derecesi, B den oluşan elektronların kütle hareketi etkisiyle zayıflar. Bu koşullar altında iyonizasiyon derecesini saptamak için B nin disosiyasyon sabiti ve kütle-dengesinden bir hesaplama yapılması gerekir.
Alevlerde atom-iyon dengesinin bulunması, alev
spektroskopisinde pek çok önemli sonuç doğurur. Örneğin, alkali metallerin
(özellikle potasyum, rubidyum ve sezyum) atomik emisyon veya absorbsiyon
hatlarının şiddetleri sıcaklıktan karmaşık bir biçimde etkilenir. Artan
sıcaklıklar, Boltzmann denklemine göre uyarılmış atomların artmasına neden
olur; bu etkiye karşın, iyonizasyonla oluşan atomların konsantrasyonu azalır.
Böylece, bazı koşullarda daha yüksek alevlerde emisyon veya absorbsiyonda
azalma gözlenir. Alkali metallerin analizlerinde düşük uyarılma sıcaklıklarının
kullanılması bu nedenledir.
İyonizasyon denklemlerindeki kaymalar bir "iyonizasyon
durdurucu" ile önlenebilir. Bu tür bir madde aleve yüksek konsantrasyonda
elektronlar verir ve analitin iyonlaşmasını engeller. Bu durdurucun etkisi,
stronsyum için, Şekil-14'de verilen kalibrasyon eğrisiyle gösterilir. Potasyum
iyonları ve elektronların konsantrasyonları arttırılarak stronsyumun
iyonizasyonu azaltıldıkça eğrilerin dikliği artmaktadır. Ayrıca oksitleyici olarak
hava yerine azot oksit kullanıldığında hassasiyetin artığı da görülmektedir; bu
durum azot oksit ile daha yüksek sıcaklığa ulaşıldığından plazmadaki stronsyum
bileşiklerinin bozunma ve buharlaşma hızının artmasından ileri gelir.
Şekil-14: Stronsyumun kalibrasyon
eğrisine potasyum konsantrasyonunun etkisi
Analitik Yöntemler
Atomik absorbsiyon spektroskopide hem kalibrasyon eğrileri
yöntemi hem de standart katma yöntemi kullanılır.
Kalibrasyon Eğrileri
Teorik olarak absorbansın konsantrasyonla orantılı olması
gerektiği halde çoğu zaman doğrusallıktan sapmalar olur. Bu nedenle kalibrasyon
eğrilerine gereksinim vardır. Ayrıca, analizin yapıldığı zaman en az bir
standardın absorbansı tekrar ölçülerek atomik buhar elde edilirken kontrol dışı
kalan değişkenlerin neden olduğu hatalar saptanır. Böylece standardın orijinal
kalibrasyon eğrisinden gösterebileceği sapma, örnek için elde edilen sonuçların
düzeltilmesinde kullanılır.
Standart Katma
Yöntemi
Standart katma yöntemi absorbsiyon spektroskopisinde çok
kullanılır. Bu yöntemde iki veya daha fazla örnek çözeltisi eşit hacimlerdeki
volumetrik balonlara alınır. Bunlardan biri çözeltisi ile balon hacmine
tamamlanır ve absorbansı okunur. İkinci balona önce bilinen miktarda analit
ilave edilir ve sonra aynı hacme seyreltilerek absorbansı okunur. Diğer
balonlara da aynı şekilde bilinen miktarlarda standardlar ilave edilip,
absorbans değerleri saptanarak istenildiği kadar veri toplanabilir. Eğer
absorbans ve konsantrasyon arasında doğrusal bir ilişki varsa, aşağıdaki denklemler
uygulanabilir.
Burada Cx seyreltilen örnekteki analit
konsantrasyonu, Cs ilave edilen standardın konsantrasyona getirdiği
artışı gösterir. Ax ve AT ölçülen absorbans değerleridir.
İki denklemin birleştirilmesiyle aşağıdaki eşitlik elde edilir.
Değişik miktarlarda standart ilave edilerek bir kaç çözelti
hazırlanması durumunda AT ve
Cs grafiğe alınır ve elde
edilen doğru AT= 0’a ektropole edilerek elde edilen değer Denklem(5)’de yerine konursa Cx =-
Cs bulunur.
Standart katma yönteminde, örnek çözeltisindeki fiziksel ve
kimyasal bazı etkenlerden kaynaklanan hatalar birbirini giderirler.
Organik Çözücülerden
Yararlanma
Alev absorbsiyonu ve emisyonu piklerinin yükseklikleri düşük
molekül ağırlıklı alkoller, ketonlar, ve esterlerin bulunduğu ortamlarda (su
olsun veya olmasın) artar. Bu etki, nebulizer veriminin artmasıyla açıklanır;
söz konusu organik maddelerin yüzey gerilimlerinin düşük olması, damlaların
daha küçük olmasına ve aleve ulaşan örnek miktarının artmasına neden olur.
Organik çözücülerle daha zayıf yakıt-oksitleyici oranları
kullanılarak ilave edilen organik maddenin etkisi azaltılmalıdır. Bu durumda da
alev sıcaklıkları düşük olacağından kimyasal
girişim olasılığı artar.
Alev spektroskopisinde organik çözücülerle çalışma, en çok
analitin suda çözünmeyen bir organik madde ile çekilmesi durumunda uygulanır.
Burada dithizon veya 8-hidroksikınolin gibi şelat yapıcı bir madde ile analit
iyonları organik çözücüde çözünür hale dönüştürülür. Elde edilen organik
ekstrakt doğrudan aleve verilir ve atomik absorbsiyonu, emisyonu veya
fluoresansı ölçülür.
ATOMİK EMİSYON
SPEKTROSKOPİSİ
Atomik emisyon spektroskopisi (aynı zamanda alev emisyon
spektroskopisi veya alev fotometresi de denir) elementel analizlerde çok
kullanılır. En yaygın kullanım yerleri, özellikle biyolojik sıvılar ve
kültürlerde sodyum, potasyum, lityum, ve kalsiyum analizleridir. Kolaylığı,
sürati ve kısmen de olsa girişim etkilerinin azlığı nedeniyle alev emisyon
yöntemi tercih edilir. Periyodik sistemdeki elementlerin yarıya yakını bu
yöntemle (farklı hassasiyetlerde) analiz edilebilirler. Bu da alev emisyon
spektrofotometresinin analizlerde kullanılan en önemli cihazlardan biri olduğunu
gösterir.
Alev emisyonu çalışmalarında kullanılan cihazlar, alev
absorbsiyonu cihazlarına benzer, aradaki fark emisyonda alevin ışın kaynağı
olmasıdır; bu nedenle oyuk katot lambası ve choppere gerek yoktur. Modern
cihazların çoğu emisyon veya absorbsiyon analizlerinde kullanılabilecek şekilde
dizayn edilmişlerdir. Atomik emisyon analizlerinin çoğunda önceleri türbülent
akışlı bekler kullanılırdı. Yeni cihazlardaki bekler çoğunlukla laminar
akışlıdır.
Spektrofotometreler
Rutin olmayan analizlerde ayırma gücü ~0.5 A0
olan kaydedicili bir UV-görünür spektrofotometre uygundur.
Fotometreler
Alkali ve toprak-alkali metallerin rutin analizleri için
basit filtreli fotometreler yeterlidir. Diğer metallerin çoğunun uyarılması
düşük-sıcaklıklı alev kullanılarak önlenir. İstenilen emisyon hattı cam veya
girişim filtreler ile ayrılır.
Bazı cihaz imalatçıları kan serumu ve diğer biyolojik
örneklerde NA, K ve Lİ analizlerinde kullanılan alev fotometreleri
yapmaktadırlar. Bu cihazlarda alevden gelen ışın yaklaşık olarak eşit güçlerde
üç kısma ayrılır. Bunlardan her biri, bir girişim filtresi (bu filtre
elementlerden birinin emisyon hattını geçirirken diğer ikisine ait olanları
absorblar), foto tüpü ve bir amplifieri bulunan ayrı birer fotometrik sisteme
girer. Sistemlerin çıkışları ayrı ayrı ölçülebilir. Analizlerde Li çoğunlukla
bir iç standard olarak kullanılır. Bu amaçla her standard ve örneğe sabit
miktarda Li konur. Na ve Li transdüseri ile K ve Li transduserinin çıkış
sinyallerinin oranları analitik parametrelerdir. Böyle bir sistemin doğruluğu
oldukça yüksektir. Çünkü üç hattın şiddetleri alev sıcaklığı, yakıt akış
hızları ve taban ışınları gibi analitik değişkenlerden aynı derecede
etkilenirler. Böyle bir çalışma örnekte Li elementi bulunmadığı halde
yapılabilir.
Otomatik Alev
Fotometreler
Kliniklerdeki tam otomatik fotometrelerde dönen bir örnek
tablası vardır ve örnek buradan sırayla alınır, protein ve asılı taneciklerin
ayrılması için diyaliz edilir, Li standardıyla seyreltilir ve aleve
püskürtülür. Örnek ve kimyasal maddelerin taşınması bir döner-tip pompa ile
yapılır. Örnekler hava kabarcıklarından yararlanılarak birbirinden ayrılır.
Sonuçlar bir kağıt şerit üzerine kaydedilir. Her 9 örnekten sonra otomatik
olarak kalibrasyon işlemi tekrarlanır.
Çok Sayıda Elementin
Hızlı Analizinde Kullanılan Cihazlar
1970'li yıllarda bir örnek içindeki bir kaç elementi ardışık
(ardarda) veya eşzamanlı analiz eden cihazların geliştirilmesi üzerinde yoğun
çalışmalar başlatılmıştır. Bunlardan biri de Na va K analizinde kullanılan basit
bir fotometredir. Çalışmalar bilgisayar kontrollü monokromatörler üzerinde
yoğunlaştırılarak, çeşitli elementlerin piklerini tanımlayan dalga boylarındaki
ışın gücünün ardarda ölçülmesi gerçekleştirilmiştir. Bu tip cihazlarda bir
pikden diğerine geçiş için iki-üç saniye gibi çok kısa bir süre yeterli
olabilmektedir. Böylece bir dakika içinde 10 kadar elementin konsantrasyonu
tayin edilebilir. Bu tip cihazlar üç alev yöntemiyle de çalışabilir. Emisyon
yöntemi, kaynağa gereksinim olmadığından diğerlerine tercih edilir.
"Eşzamanlı", çok sayıda element analizlerinin
yapıldığı alev emisyon yöntemlerinde optik çok-kanallı analizörler kullanılır.
Örneğin, her hangi bir grating monokromatör slitinin bulunduğu optik düzlem
üzerine bir slikon diod vidicon tüp konur. Tüp yüzeyinin çapı, 20 nm'lik ışın
bandını izleyebilecek büyüklüktedir; tüpün monokromatör merkez düzlemi boyunca
yerleştirilmesiyle spektrumun 20 nm'lik (ayırma gücü ~0.14 nm) çeşitli bandları
gözlenebilir. Şekil-15 de, 388.6-408.8 nm dalga boyu aralığında emİsyon pikleri
bulunan 8 elementin eşzamanlı spektrumu görülmektedir. Uyarıcı azot oksit/
asetilen alevidir. Bu 8 analizin verileri yarım dakikadan daha az bir sürede
alınmıştır, relatif hassasiyet %5 dolaylarındadır. (Relatif güç: bağıl yayım
şiddetini belirtir.)
Alev emisyon spektroskopisinde karşılaşılan girişimlerler,
atomik absorbsiyondaki nedenlerden kaynaklanır; ancak şiddetleri birbirinden
farklıdır.
Spektral Hat Girişimi
(Engellemesi)
İki atomik absorbsiyon pikinin üst üste düşmesi (bu durumda
birbirini engellerler) sadece piklerin dalga boyları arasında 0.1 A kadar küçük
bir farklılık olması halinde gözlenir; böyle bir durumla ise nadiren
karşılaşılır. Burada spektral seçicilik, monokromatörün yüksek ayırma gücünden
çok, kaynağın verdiği dar hat özelliğinin bir sonucudur. Oysa atomik emisyon
spektroskopide seçicilik tümüyle monokromatöre bağlıdır; bu nedenle de piklerin
üst üste düşmesiyle doğan engelleme atomik emisyonda daha büyüktür. Şekil-16'da
demir, nikel ve krom geçiş elementlerinin emisyon spektrumu görülmektedir.
Burada bazı ayrılmamış piklerin bulunduğunun ve bu elementlerden herhangi
birinin analizinde spektral girişim ile karşılaşılabileceğinin bilinmesi
gerekir.
Şekil-15: Çok elementli alev emisyon
spektrumu; 388.6-408.6 nm aralığında
Şekil-16: 600 ppm Fe, 600 ppm Ni ve
200 ppm Cr içeren bir örneğin
kısmi oksihidrojen alev emisyon spektrumu
Band Engellemesi;
Zemin (Background)) Düzeltmesi
Emisyon hatları çoğunlukla, örnek, yakıt, veya
oksitleyiciden oluşan oksitler veya diğer moleküler tanecikler tarafından emitlenen
bandlar üzerine düşerler (Şekil-17). Şekilde görüldüğü gibi band emisyonu için,
analit pikinin başladığı ve bittiği iki ucunda, bir kaç angström birimlik
bölgede zemin düzeltmesi yapılır. Kaydedicisi bulunmayan cihazlarda ise pikin
iki ucunda ölçme yapılması yeterlidir. Bu iki değerin ortalaması alınarak
toplam pik yüksekliğinden çıkarılır.
Kimyasal Girişimler
(Engellemeler)
Alev emisyonu çalışmalarında karşılaşılan kimyasal
girişimler, alev absorbsiyonu yöntemlerinde karşılaşılanlarla aynıdır. Alev
sıcaklığının bilinçli olarak seçilmesi ve koruyucu, uzaklaştırıcı, ve
iyonizasyon önleyiciler kullanılarak bu sorunlardan kurtulunmaya çalışılır.
Öz Soğurma (Kendini -
Absorblama)
Bir alevin merkezi dış çevresinden daha sıcaktır; bu nedenle
merkezde oluşan atomlar, yüksek konsantrasyonda uyarılmamış atomlar içeren daha
soğuk bir bölge ile çevrilmişlerdir; sonuçta soğuk tabakadaki atomlar resonans
dalga boylarını absorblarlar (öz soğurma). Emisyon hattının Doppler genişlemesi,
buna karşı gelen resonans absorbsiyon hattının genişlemesinden daha büyük olur,
yine de tanecikler daha sıcak-emisyon bölgesinde, daha hızlı hareket ederler.
Böylece, öz soğurma, bir hattın merkezini kenarlarına kıyasla daha fazla
değiştirir. En şiddetli halde ise merkez, kenarlardan daha az şiddette olur,
hatta kaybolabilir; sonuçta emisyon maksimumu kendini-çevirerek iki pik oluşur.
Şekil-18'kendi kendini absorbsiyon ve kendini-çevirme olayını göstermektedir.
Öz soğurma çoğunlukla analitin konsantrasyonunun yüksek
olması durumunda ortaya çıkar. Bu gibi hallerde analiz için resonans olmayan
hatlar kullanılır; çünkü bu hatlar aynı etkiye uğramazlar.
Şekil-18: A, yüksek konsantrasyonda
Mg (200 mg) bulunduğunda ters dönme, B 100
mg Mg’un normal spektrumu
Şekil-19: Potasyumun
kalibrasyon eğrisinde iyonizasyon ve
kendi kendini absorblamanın etkileri
Öz soğurma ve iyonizasyon, bazan üç bölgeli S şeklinde
emisyon kalibrasyon eğrileri verirler. Potasyumun orta derecelerdeki
konsantrasyonlarında, ışının şiddeti ile konsantrasyon arasında doğrusal bir
ilişki gözlenir (Şekil-19). Düşük konsantrasyonlarda doğrunun hafifçe eğilmesi
alevdeki iyonizasyon derecesinin artmasından kaynaklanır. Diğer taraftan, yüksek
konsantrasyonlarda doğrudan negatif bir sapma gözlenir ki bu durum da kendi
kendini absorblama özelliğinden dolayıdır.
Alev emisyon spektroskopide uygulanan analitik yöntemler,
daha önce görülen atomik absorbsiyon uygulamalarına benzer. Bunda da hem kalibrasyon
eğrileri, hem de standart katma yöntemleri kullanılır. Ayrıca alevdeki
değişiklikleri giderebilmek için iç standartlar da kullanılabilir.
Atomik Emisyon ve
Atomik Absorbsiyon Yöntemlerinin
Kıyaslanması
Kıyaslanması
Çok geniş bir kullanım alanı olan bu iki alev yönteminin
avantaj ve dezavantajları aşağıda sıralanmıştır. Kıyaslamalar, çok sayıda
elementin analiz edildiği çok maksatlı spektrofotometreler için geçerlidir.
1. Cihazlar: Emisyon yöntemiyle çalışan cihazların en önemli
avantajı alevin kaynak görevi yapmasıdır. Tersine, absorbsiyonda her element
(veya bir grup element) için özel bir
lamba gerekir. Diğer taraftan, bir absorbsiyon cihazının monokromatörünün çok
üstün kalitede olmasına gerek yoktur, çünkü yüksek seçicilik, oyuk (hallow)
katot lambasından çıkan dar hatlarla sağlanır.
2. Operatörün Yeteneği : Emisyon yöntemlerinde dalga boyu,
örneğin alevin neresinde bulunması gerektiği, ve yakıt/oksitleyici oranı gibi
kritik ayarların önemi nedeniyle operatör yeteneği önemli bir faktördür.
3. Zemin Düzeltmesi: Örnekteki maddelerden kaynaklanan band
spektralarını gidermek için uygulanan zemin düzeltmesi işlemi emisyon
yöntemlerinde daha kolay ve daha doğru olarak yapılabilir.
4. Duyarlık ve Doğruluk :Deneyimli operatörlerin
çalışmalarında her iki yöntemin de hassasiyet ve doğruluğu aynıdır (%± 0.5-1).
Operatörün deneyiminin azsa atomik absorbsiyon yönteminde başarı daha yüksek
olur.
5. Girişimler: İki yöntemde de benzer kimyasal girişimlerle
karşılaşılır. Atomik absorbsiyonda spektral hat girişimleri daha azdır.
Emisyonda bu tip girişimlerin daha fazla olmasına karşın, bunların kolayca yok
edilebilmeleri mümkündür. Spektral band
girişimleri zemin düzeltmesi ile giderilebilir.
6. Tayin Sınırları: Tablo-5'de iki yöntemin tayin
edilebileceği elementler ve duyarlıkları gösterilmiştir.
Tablo-5: Alev Absorbsiyonu ve Alev Emisyonu Yöntemlerinde
Çeşitli Elementler İçin Tayin Sınırlarının Kıyaslaması

Çeşitli Elementler İçin Tayin Sınırlarının Kıyaslaması

ATOMİK FLUORESANS
SPEKTROSKOPİSİ
1966'dan bu yana atomik fluoresans spektroskopinin ilkeleri
ve uygulamaları üzerinde yoğun araştırmalar yapılmaktadır. Çalışmalar bu
yöntemin (özellikle alevsiz çalışmaların uygun bulunduğu) 5-10 element için
diğer iki alev yöntemine göre daha hassas olduğunu göstermiştir. Pek çok
element için ise atomik fluoresans yönteminin hassasiyeti pek iyi değildir ve
ancak düşük konsantrasyonlarda uygulanabilir. Ayrıca fluoresans cihazları çok
karmaşık ve bu nedenle de gerek satış fiyatı ve gerekse bakımı oldukça pahalıdır.
Cihaz
Atomik fluoresans cihazında zayıf bir kaynak, bir atomizer
(alevli veya alevsiz), bir monokromatör veya bir girişim-filtre sistemi, bir
dedektör, ve bir sinyal-çalıştırma sistemi bulunur. Kaynağın dışındaki diğer
kısımlar bu bölümde daha önce tarif edilen aynı fonksiyonlu parçalara benzer
özelliktedir.
Atomik fluoresans ölçmelerinde sürekli bir kaynak tavsiye
edilir. Ancak bir atomik hat genişliği kadar dar bir bölgeyi kapsayan sürekli
bir kaynağın çıkış gücü çok düşüktür ve yöntemin hassasiyetini azaltır.
Bilinen oyuk (hallow) katot lambaları (sürekli olarak
çalıştırılır) fluoresans analizler için gerekli ışın gücünü veremezler. Bu
lambalara kısa periyotlarda büyük akımlar verilerek şokla çok şiddetli ışın
enerjileri elde edilebilir. Ancak lambaların tahrip olmaması için periyodların
ve akımın miktarında dikkatli olunması gerekir. Fluoresansı algılayacak
dedektör sadece şok uygulandığı sırada devrede olmalıdır.
Fluoresans ölçmeleri için gerekli ışın gücünü verebilecek
gaz-boşaltma lambaları da vardır; bunlar alkali metaller, civa, kadmiyum,
çinko, talyum, ve galyum gibi çok uçucu bazı elementlerin tayininde
kullanılabilir.
Elektrodsuz boşalım lambaları da çeşitli elementler için çok
şiddetli hat veren kaynaklardır. Bu lambalarda yaklaşık 1 torr basınçlı bir
inert gaz ile analizi yapılacak elementin bir tuzu veya kendisi bulunur.
Uyarılma, tüp bir mikro dalga alana konularak sağlanır; mikro dalga alan bir
anten veya yansıtıcı ile oluşturulur.
Atomik fluoresans çalışmalarda kaynak olarak ses dalgaları
veren lazerlerin kullanılmasına da başlanmıştır.
Atomik fluoresans spektroskopide karşılaşılan girişimler,
absorbsiyon spektroskopide karşılaşılanlarla aynı tipte ve hemen hemen aynı
büyüklüktedir.
Atomik fluoresans yöntemleri yağlama yağları, deniz suyu,
grafit, ve zirai ilaçlarda bulunan metallerin analizlerinde kullanılır.